通信作者:居漪,Email:juyi@sccl.org.cn
【摘要】 目的 基于电感耦合等离子体质谱法(ICP‐MS),建立一种检测血清钙离子的候选参考方法。方法 方法学建立.将从医院收集到的血清标本以0.3%硝酸溶液直接稀释100倍,在血清标本基质溶液中添加不同浓度钙标准溶液,配制含血清基质的标准品溶液。以锗(Ge)为内标,采用标准加入法,计算血清钙离子浓度。对所建立的候选参考方法进行线性、精密度、正确度的性能评估和方法比对。结果 血清钙离子浓度在0.000~20.400 mmol/L内(稀释后浓度为0.000~0.204 mmol/L)线性良好(R2>0.999 9);批内不精密度为 0.22%~0.47%,批间不精密度为 0.64%~0.77%,总不精密度为0.98%~1.09% ;检测 3 个浓度 SRM 956d,结果均在证书要求的不确定度范围内,相对偏移分别为-0.16%,0.04%,0.23% ;该方法参加2017年参考实验室外部质量评价计划(RELA),比对通过。与检验医学溯源联合委员会(JCTLM)所列参考方法进行比较,结果一致性良好。本研究所建立的候选参考方法与临床常规电极方法进行比较,具有良好的相关性。结论 成功建立血清钙离子检测候选参考方法,线性范围宽、具有良好的精密度与准确度。
【关键词】 钙; 质谱分析法; 参考标准
DOI:10.3760/cma.j.issn.1009‐8158.2020.01.006
Department of Reference Measurement Laboratory, Shanghai Center for Clinical Laboratory, Shanghai200126, China
Corresponding author: Ju Yi, Email: juyi@sccl.org.cn
【Abstract】 Objective To establish a candidate reference method for serum calcium determination based on inductively coupled plasma mass spectrometry(ICP‐MS).Methods Establishment of methodology: serum samples collected from the hospital were diluted 100 times by 0.3% ultrapure nitric acid. Calcium standard solutions with different concentrations were added to serum samples matrix solutions. Serum calcium concentration was calculated according to the standard addition method using germanium(Ge) as internal standard. The linearity, precision,trueness of the performance of the established candidate reference method were evaluated, and a comparison with the reference method was made. Results The linearity was good in serum calcium concentrations from 0.000 mmol/L to 20.400 mmol/L (the concentration after dilution from 0.000 mmol/L to 0.204 mmol/L) (R2>0.999 9);the within‐run precision was from 0.22% to 0.47%, and the between‐run precision was from 0.64% to 0.77%; the total precision was from 0.98% to 1.09%. The determination results of 3 concentrations of SRM 956d were all in the uncertainty range required by the certificate. The biases were - 0.16%, 0.04% and 0.23%, respectively. The established candidate reference method participated in and passed the 2017 External Quality Assessment Scheme for Reference Laboratories in Laboratory Medicine (RELA) comparison. The results of the established candidate reference method were consistent well with those of the reference method in the Joint Committee for Traceability in Laboratory Medicine(JCTLM)list. There was a good correlation between the established candidate reference method and the clinical routine electrode method. Conclusions The established candidate reference method for serum calcium determination based on ICP‐MS is precise, accurate, with wide range of linearity.It is expected to play a role in tracing the quantities of serum calcium in clinical laboratories.
【Key words】 Calcium; Mass spectrometry; Reference standards
DOI:10.3760/cma.j.issn.1009‐8158.2020.01.006
人体内的总钙包括游离钙和结合钙,在反应体内钙总体代谢状况上,需对总钙进行检测[1]。血清钙常规检测方法主要是离子选择性电极法、化学试剂盒法等,在临床实验室中不同原理的常规分析方法会产生不一致的结果,参考方法的重要性已经得到广泛的认可[2‐3]。目前检验医学溯源联合委员会(Joint Committee for Traceability in Laboratory Medicine,JCTLM)推荐的检测血清中钙的参考方法有 同 位 素 稀 释 热 电 离 质 谱 法(Isotope Dilution Thermoionization Mass Spectrometry,ID‐TIMS)[4]、离子色谱法(Ion Chromatorgaphy,IC)[5]、火焰原子吸收光谱法(Flame Atomic Absorption Spectrometry,FAAS)[6]、电感耦合等离子体发射光谱法(Inductively Coupled Plasma Emission Spectrometry,ICP‐OES)[7]、同位素稀释电感耦合扇形磁场质谱法[Isotope Dilution Inductively Coupled Sector Magnetic Field Mass Spectrometry, ICP‐(ID)SFMS][8] 、同位素稀释电感耦合等离子体质谱法(Isotope Dilution Inductively Coupled Plasma Mass Spectrometry,ID/ICP‐MS)[9] 、电感耦合等离子体质谱法 (Inductively Coupled Plasma Mass Spectrometry,ICP‐MS[10]。
血清钙检测决定性方法是同位素稀释质谱法,但此法因金属同位素价格昂贵、货源稀少、仪器操作复杂等原因应用较少。近年来ICP‐MS以其线性范围宽、检测灵敏度高、操作简便等优点得到广泛的关注[11]。Ying等[10]以铝元素为内标建立了血清钙离子检测的 ICP‐MS 参考方法 ,该方法已被JCTLM收录为参考方法。本研究应用ICP‐MS为测量工具,基于标准加入法[12]和内标锗相结合建立一种精密度准确度良好、操作简便、安全快速的血清钙离子候选参考方法。
(一)标本
收集 2019 年 1 月至 3 月上海市东方医院门诊及住院患者,取静脉血3 ml的单一新鲜血清标本,保存于-80 ℃。
(二)仪器
PE 300X 型电感耦合等离子体质谱仪(美国珀金埃尔默公司);Mettler AX205 万分之一(Max=200g,d=10-4g)天平(德国梅特勒‐托利多公司);Milli‐Q超纯水机(法国 Millipore公司);可控温电热板(美国 LabTech 公司);cobas c 702 生化仪(瑞士罗氏公司)。
(三)试剂
美国国家标准物质NIST 3109a,证书值:9.819mg/g;不确定度:0.019 mg/g;NIST 956d 水平1,水平2,水平3;锗Ge(国家标准物质研究院),浓度1000μg/ml;浓度69%的光谱级高纯硝酸购自美国赛默飞世尔实验器材有限公司;实验使用的超纯去离子水(18×106Ω•cm)由Mill‐Q纯水机制得。
二、方法
(一)ICP‐MS方法参数建立和优化
1. ICP‐MS 质 谱 仪 条 件 :ScanMode:Peak Hopping,Dwell Time=100 ms,Integration=3 000 ms,Analysis Mode:KED,He gas flow rate=3 ml / min,Rpa=0, Rpq=0.25, Sweeps=30,Readings=1,Replicates=3。
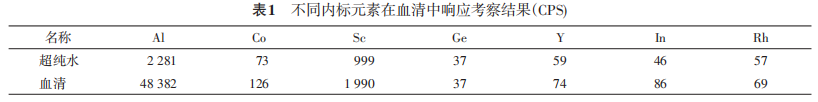
2. 内标考察与选择:用 ICP‐MS 分别考察血清中与超纯水中钪(Sc)、锗(Ge)、铱(Y)、铟(In)、铑(Rh)及铝(Al)、钴(Co)的响应信号值CPS,选择血清和水中响应较小且符合性较一致的物质作为内标。
(二)检测前处理
1. 溶剂(0.3%硝酸溶液)、钙标准物质储备液、内标液的配制:分别由69%超纯硝酸、NIST 3109a、锗标准溶液稀释制得。
2. 工作标准溶液的配制:空白溶液:0.3%硝酸溶液;待测标本:精密称量0.5 g标本和0.5 g内标液通过重量法用溶剂稀释100倍;加标溶液1:自待测标本中精密称量10.0 g溶液于离心管中,精密加入0.05 g标准物质储备液;加标溶液2:自待测标本中精密称量10.0 g溶液于离心管中,精密加入0.1 g标准物质储备液;加标溶液 3:自待测标本中精密称量10.0 g溶液于离心管中,精密加入0.2 g标准物质储备液。
(三)性能评估
1. 线性评价:本研究的线性评价是针对校准曲线的线性进行评价。
2. 精密度:每天检测两个浓度的标本,每个浓度标本检测3次,连续检测5 d。
3. 正确度:通过检测 NIST SRM956d 3 个水平浓度来考察检测方法的正确度(每个浓度重复检测3次);用所建立的方法参加了2017年度国际临床化学和医学实验室联合会(International Federation of Clinical Chemistry and Laboratory Medicine,IFCC)组织的参考实验室室间质量评价(External quality control for Reference Laboratories,RELA)。
(四)方法比对
在本实验室运行了JCTLM列表中国际公认的血清钙离子参考测量方法,参照文献[10],用两种方法对 20 份标本进行检测比较;与临床常规离子选择性电极法检测40份标本进行比较。
(五)结果计算
利用校准品拟合方程 Y=kX+b,计算出 k 值(Y是校准品中Ca的响应信号与内标Ge信号的比值,X是Ca的浓度值);实际标本中血清钙含量的计算公式如下:
C=(k×n×D×V)( I×1 000×40.078);C:血清中Ca的实际浓度mmol/L;n:标本稀释倍数;D:血清密度;V:冻干血清标本的复溶因子,复溶水的质量/(规定复溶水的体积×实验温度下水的密度);I:待测标本中钙的信号与内标信号的比例;40.078:Ca的平均相对分子质量。
结 果
一、内标元素考察与选择
对不同元素在超纯水与水清中响应信号进行考察,可以发现Ge在超纯水和水清中的响应信号均最小且都为37 CPS,说明Ge在超纯水和血清中的含量均很小。因此,应选用 Ge 作为内标,结果见表1。
二、线性评价
以浓度为X,对应钙元素信号CPS与内标信号CPS 比值为 Y,见图 1,在 0.000~8.000 μg/g(0.000~0.204 mmol/L)钙离子浓度范围内建立线性回归方程,对应稀释前浓度范围是 0.000~20.400 mmol/L,Y=0.943 2X+0.7212,R2=0.999 95,标准曲线的相关系数>0.999 9。
三、精密度
采用高低两个浓度的临床血清标本考察方法的精密度,用批内不精密度、批间不精密度及总不精密度表示,不精密度值均小于 1.5%。结果见表2。
四、正确度
对 NIST SRM956d 水平 1、水平 2、水平 3 三个浓度的标准血清物质进行检测,结果均在认证值的不确定度范围内,见表3;2017年RELA比对实验结果见表4,两个浓度标本的测定值与靶值的相对偏移分别为-1.90%和1.46%,均在等效限(±2.50%)允许范围内。结果符合率100%。
表4 2017RELA比对实验结果
五、本实验室自建方法与参考方法的比对
用自建的候选参考方法与Ying等[10]参考方法同时检测20个浓度血清标本结果如图2。
两种方法结果线性回归方程 Passing‐Bablok: Y=1.027 4X-0.059 5(截距95%置信区间-0.161 1~0.017 0,斜率 95% 置信区间 0.993 2~1.069 7)相关性良好,线性度无明显偏差(P=0.72)。在医学决定水 平(1.75、2.74 和 3.37 mmol / L)处的偏移分别为-0.012、0.016和0.033 mmol/L
六、与临床检测方法的比对
用自建的候选参考方法与临床常规离子选择性电极法同时检测40份血清标本结果如图3。
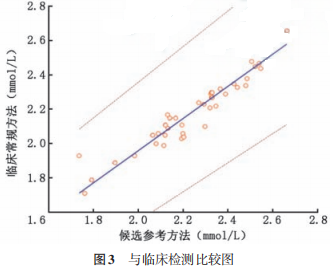
两种检测结果线性回归方程 Passing‐Bablok: Y=0.940 5X+0.079 7(截距 95% 置信区间-0.154 5~0.276 2,斜率 95% 置信区间 0.851 9~1.041 7)相关性良好,线性度无明显偏差(P=0.97)。在医学决定水 平(1.75、2.74 和 3.37 mmol / L)处的偏移分别为-0.024、-0.083和-0.121 mmol/L。
讨 论
本研究最终选择锗(Ge)作为血清钙离子检测用的内标元素是由于Ge在血清中响应与在超纯水中响应一致,在血清中含量最低,质谱干扰小,对目标分析物无干扰,且 Ge 也是推荐的内标之一[13]。在添加了内标后ICP‐MS检测血清钙离子仍然会存在两个方面的干扰因素既质谱干扰和非质谱干扰。
质谱干扰主要是因为存在与待分析物质荷比相同的干扰成分,这些干扰可以来自于载气氩气、血清标本中其他离子的干扰,这种干扰消除的方式主要有分析元素时选择质谱干扰小的同位素分析,使用高分辨率的质谱仪,使用碰撞反应气,因为高分辨率质谱仪价格昂贵限制了其使用,目前主要通过碰撞反应模式消除质谱干扰。用ICP‐MS分析钙时就存在质谱干扰,钙有6种位素40Ca(96.941%) ,42Ca(0.647%) ,43Ca (0.135%) ,44Ca(2.086%),46Ca(0.004%),48Ca(0.187%)[9],40Ca同位素丰度比最大,但易受到载气40Ar+背景干扰,44Ca易受到CO2干扰,42Ca易受到ArH干扰,48Ca易受到NO2和ArC等的干扰,本研究中选用质谱干扰相对较小的43Ca作为分析对象,且通入氦气作为碰撞气减少质谱干扰。
非质谱干扰主要是因标准物质与血清标本的基质不同。此种干扰消除的方式:标本多倍稀释,但血清标本经过100倍稀释后基质仍有影响;血清标本经过浓硝酸硝化处理,此方法可以消除血清基质中的有机物成分,但不能消除存的在无机盐类,Ying等[10]对于标本基质中剩余的无机盐进行了实验分析得出标本中的无机盐不会影响实验检测结果的结论;本研究中采用标准加入法,即在需要分析的血清标本中加入已知含量的标准溶液,依次测定标本、标本加标系列的强度,通过线性曲线中截距为 0 时的浓度值计算标本结果的方法。此法保证了待测标本和校准品的基质完全一致,消除了基质,操作简便快速,不需要经过硝化处理(时间较长需经过高温加热和赶酸且存在安全隐患)。
在建立了基于ICP‐MS血清钙离子的检测方法后,又用 20 份临床标本分别与已公认参考方法进行比对实验以及40份标本与临床常规方法比对实验,均得到了良好的相关性。说明了本研究建立的检测方法与临床常规方法是可比的,从而也为参考方法为标准物质赋值及通过参考方法评价血清钙常规检测方法的测量偏移打下基础。
综上所述,本研究建立的基于标准加入法的电感耦合等离子体质谱法检测血清中钙离子的候选参考方法相比 FAAS、ICP‐OES 等方法具有精密度高、线性范围宽、准确度好、操作简便、前处理安全快速、分析时间短等优点。开展正确度验证计划是提升临床血清钙质量控制的有效手段,该候选参考方法目前已运用在上海地区血清钙离子正确度验证计划的调查工作中。
利益冲突 所有作者均声明不存在利益冲突
参 考 文 献
[1] Jensen AC, Polcwiartek C. The Association Between Serum Calcium Levels and Short‐Term Mortality in Patiens with Chronic Heart Failure[J]. Am J Med, 2019, 132(2): 200‐208.DOI: 10.1016/j.amjmed.2018.10.006.
[2] 居漪,李卿,金中淦,等.质谱技术在参考测量程序中的应用进 展 [J]. 中 华 检 验 医 学 杂 志 , 2017, 40(10): 823‐828. DOI:10.3760/cma.j.issn.1009‐9158.2017.10.017.
[3] Zhao HJ, Ge ML, Yan Y, et al. Inductively Coupled Plasma Mass Spectrometry as a Reference Method to Evaluate Serum Calcium Measurement Bias and the Commutability of Processed Materials during Routine Measurements[J]. ChinMed J, 2018, 131(13): 1584‐1590. DOI: 10.4103 /0366‐6999.235109.
[4] Phinney CS, Murphy KE, Welch MJ, et al. Definitive methodcertification of clinical analytes in lyophilized human serum:NIST standard reference material(SRM)909b[J]. AnalChem,1998,361(2):71‐80.DOI: 10.1007/s002160050837.
[5] Thienpont LM, Van JE, Nuwenborg H, et al. Validation of candidate reference methods based on ion chromatography for determination of total calcium, potassium, calcium and magnesium in serum through comparison with flame atomic emission and absorption spectrometry[J]. Clin Biochem, 1996,29(6):501‐508.DOI:10.1016/S0009‐9120(96)00090‐2.
[6] Brown SS, Healy MJ, Kearns M, et al. Report on the inter‐laboratory trial of the reference method for the determination of total calcium in serum[J].Clin Biochem,1981,19(6):413-426.DOI:10.1079/BJN19490008.
[7] Grote‐Koska D, Klauke R, Brand K, et al. Reference measurement procedure for the determination of electrolytes in human blood via ICP‐OES measurement[J].Metrologia,2018,55(2):245‐253.DOI:10.1088/1681‐7575/aaaa3f.
[8] Kramer U, Kress M, Reinauer H, et al. Candidate reference measurement procedures for chloride, potassium, sodium, calcium,magnesium,and lithium by inductively coupled plasma(isotope dilution)sector field mass spectrometry(ICP‐(ID) SFMS) in serum[J]. Clin Lab, 2013, 59(9‐10): 1017‐1029. DOI:10.7754/Clin.Lab.2012.120902.
[9] Han B, Ge M, Zhao H, et al.Determination of serum calcium levels by 42Ca isotope dilution inductively couple plasma mass spectrometry[J].Clin Chem Lab Med, 2017, 56(1): 51‐58. DOI: 10.1515/cclm-2017‐0175.
[10] Ying Y, Menglei Ge, Rong Ma, et al. A candidate reference method for serum calcium measurement by inductively coupled plasma mass spectrometry[J]. Clinica Chimica Acta,2016,461(1)141-145.DOI:10.1016/j.cca.2016.07.004.
[11] 禹松林,程倩,韩建华,等.电感耦合等离子体质谱检测人尿液和血清中碘临床方法的建立[J]. 中华检验医学杂志,2016, 39(12): 917‐921. DOI: 10.3760 / cma. j.issn.1009‐9158.2016.12.011.
[12] Chew G, Sim LP, Ng SY, et al. Development of a mushroom powder certified reference material for calcium arsenic, cadmium and lead measurements[J].Food Chem, 2016, 190(1):293-299.DOI:10.1016/j.foodchem.2015.05.071.
[13] 中国医师协会检验医师分会临床质谱检验医学专业委员会.质谱技术在临床微量元素检测中的应用共识[S].2019,34(8):677‐681.DOI:10.3969/j.issn.1673‐8640.2019.08.001.















