在精准医疗的浪潮中,临床质谱技术凭借其高灵敏度、高特异性和多指标联检的强大优势,逐渐成为医学检验领域的 “新宠”。
在上一期,临床质谱网对获NMPA批准的质谱仪做了统计,截止到2024年底,累计有140款质谱仪获批,国内获证企业达60家。本期将为大家盘点获NMPA批准的可适用于临床检测的二类和三类质谱试剂盒,供参考。
总体概况
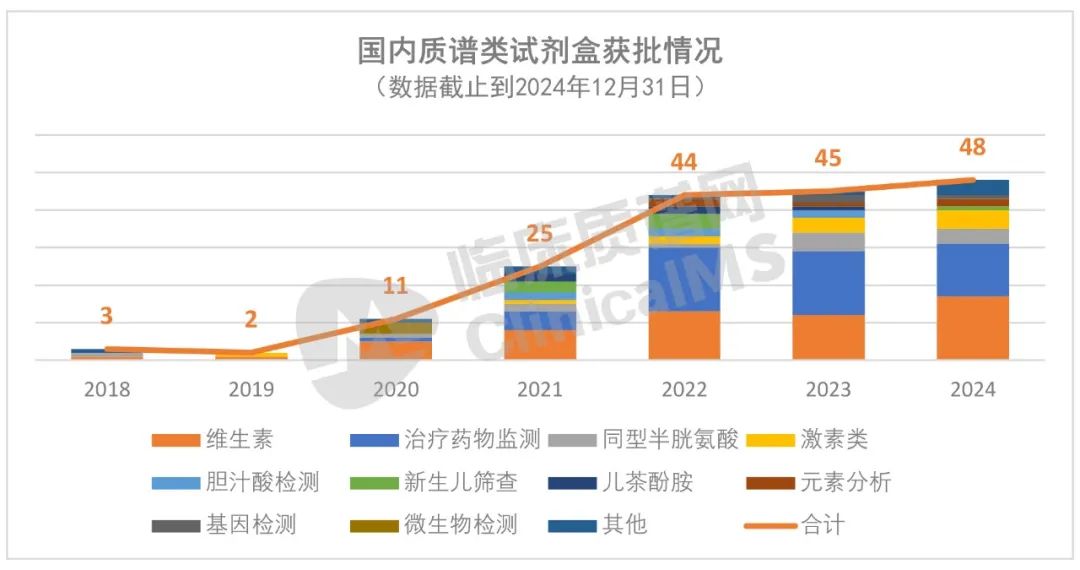
截至2024年,质谱类试剂盒注册数量累计178个,覆盖维生素、治疗药物监测、同型半胱氨酸、激素等11类检测项目。2024年单年新增注册48个(含到期更新)。已获体外诊断医疗器械注册证的试剂盒厂商有57家。
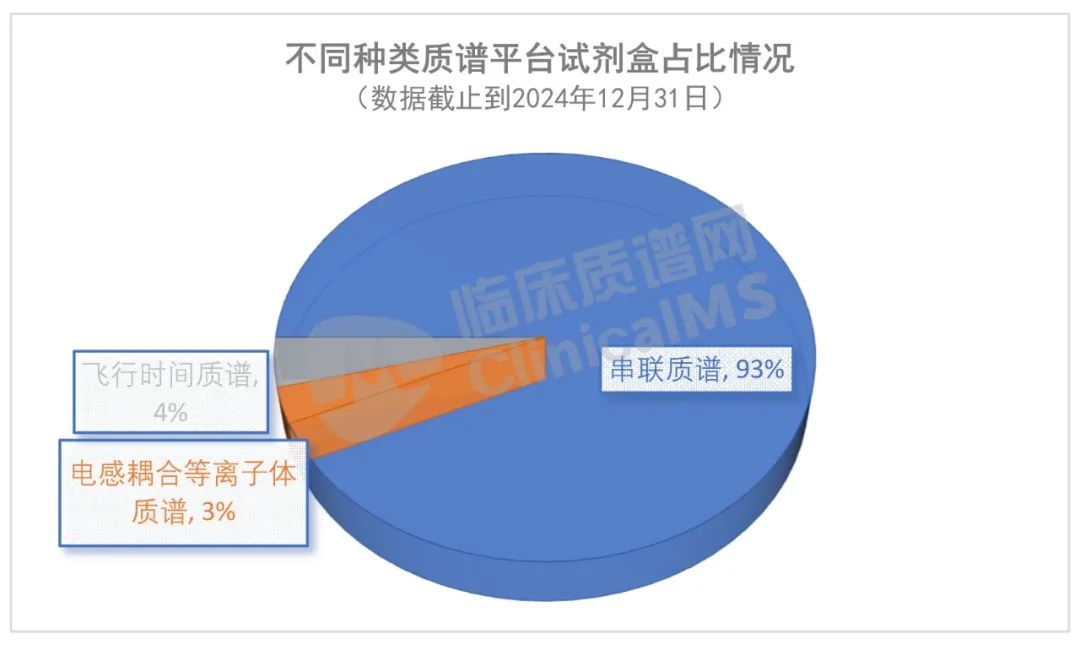
从仪器平台来看,液相色谱-串联质谱(LC-MS/MS)法试剂共166款(含进口),MALDI-TOF-MS法试剂有7款,元素分析质谱(ICP-MS)试剂有5款。93%的质谱试剂盒是基于LC-MS/MS技术平台开发的。飞行时间质谱(MALDI-TOF-MS)和ICP-MS应用场景有限,试剂盒注册数量显著低于串联质谱。
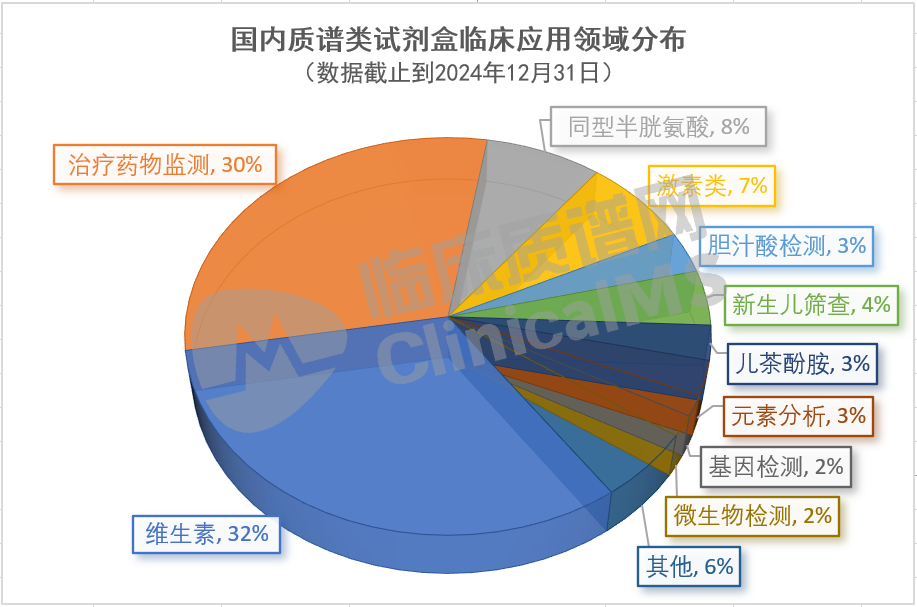
从临床应用领域来看:试剂盒注册数量占比较高的主要有维生素(57项)、治疗药物监测(54项)占比62.%,是市场核心领域;同型半胱氨酸(14项)、激素类(13项)占比15%,2023-2024年注册量稳步增长,发展潜力较大。
2023年,出现了基于飞行时间质谱的基因检测试剂盒产品,伴随肿瘤早筛、遗传病诊断需求增长,质谱技术可能成为低成本SNP检测的补充方案。目前获证的主要有以下产品:广东达瑞注册的人CYP2C19基因分型检测试剂盒(飞行时间质谱法),江苏先声诊断的二十项遗传性耳聋基因突变检测试剂盒(飞行时间质谱法),浙江迪谱诊断的人CYP2C19、ALDH2、ApoE和 SLCO1B1基因检测试剂盒(PCR-飞行时间质谱法)。
获NMPA批准的质谱法试剂盒汇总


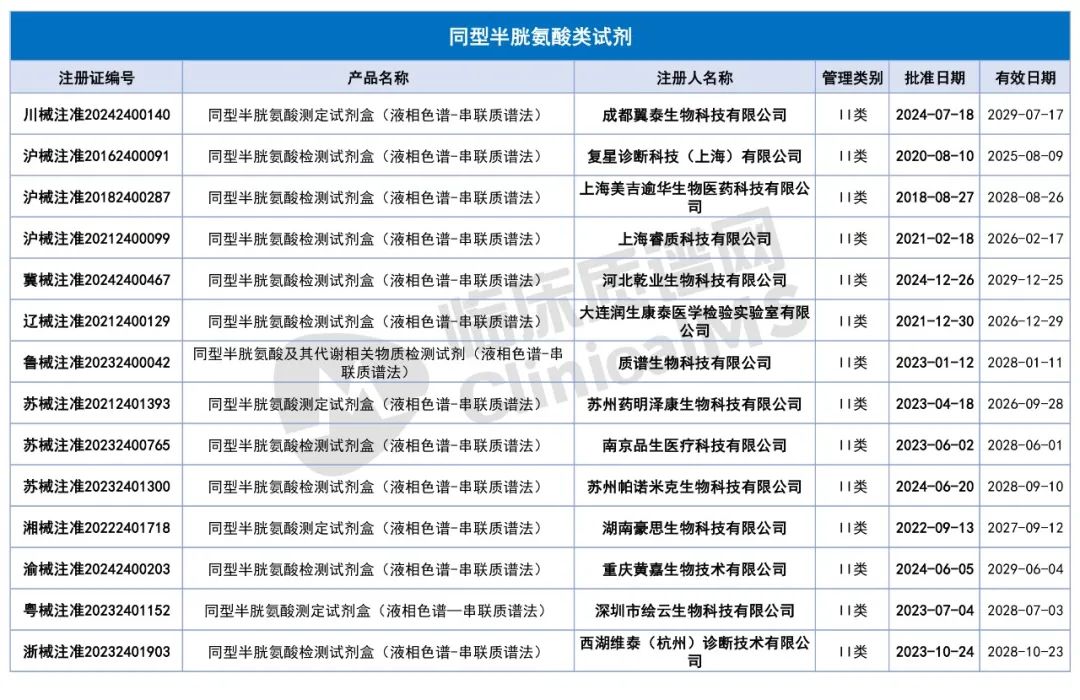
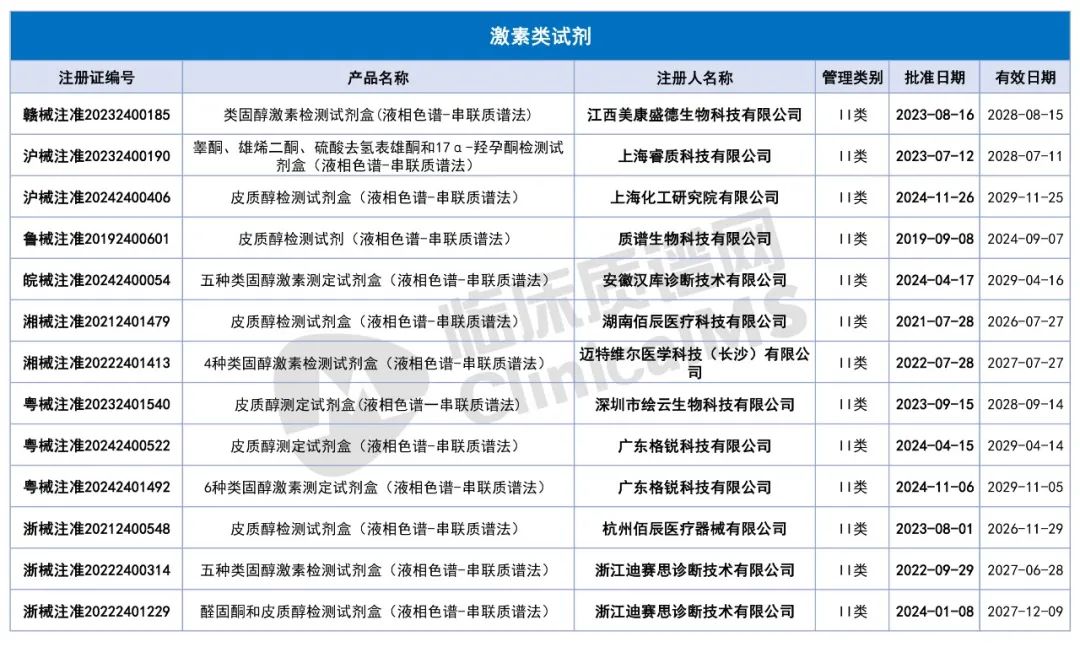
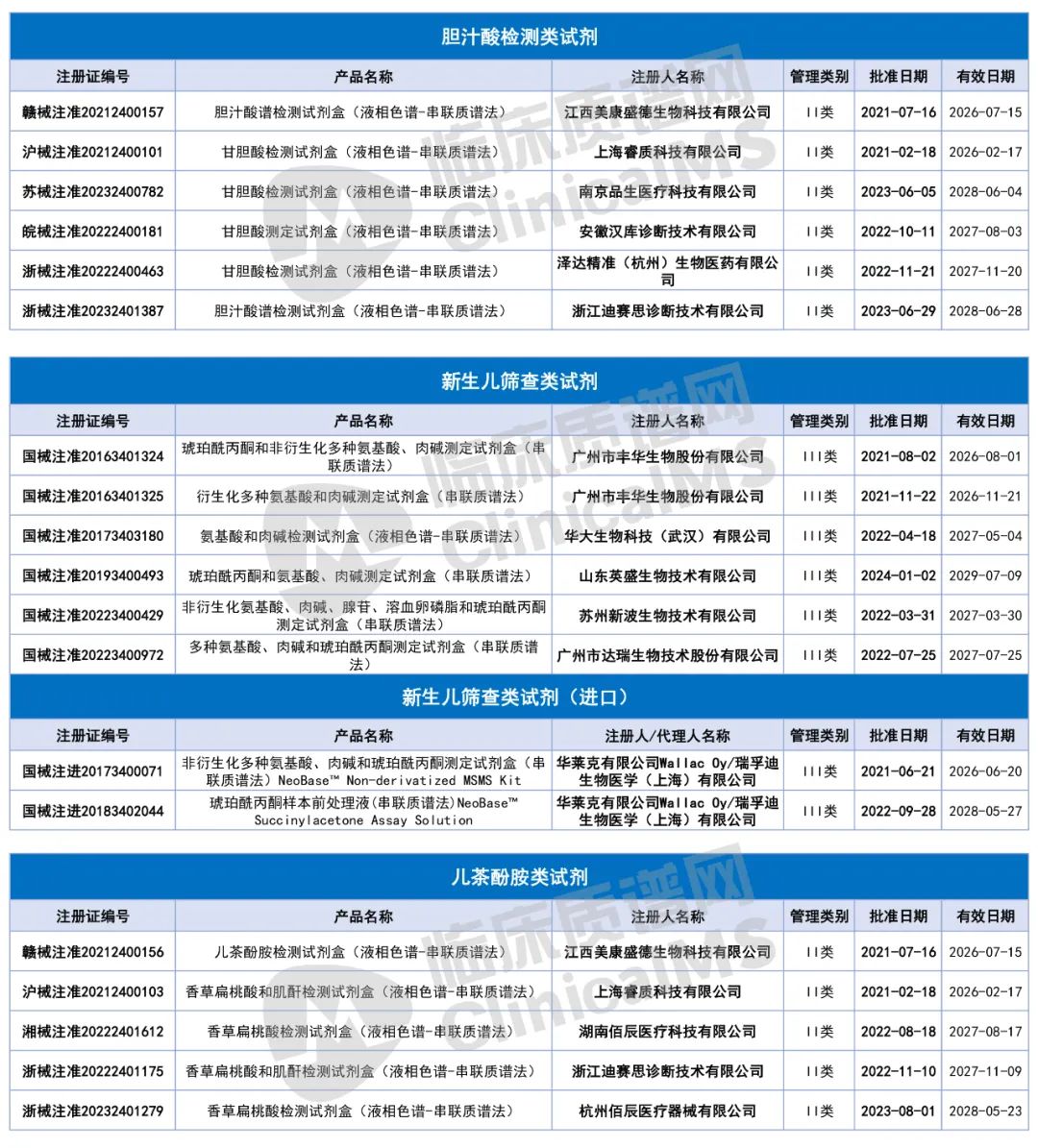
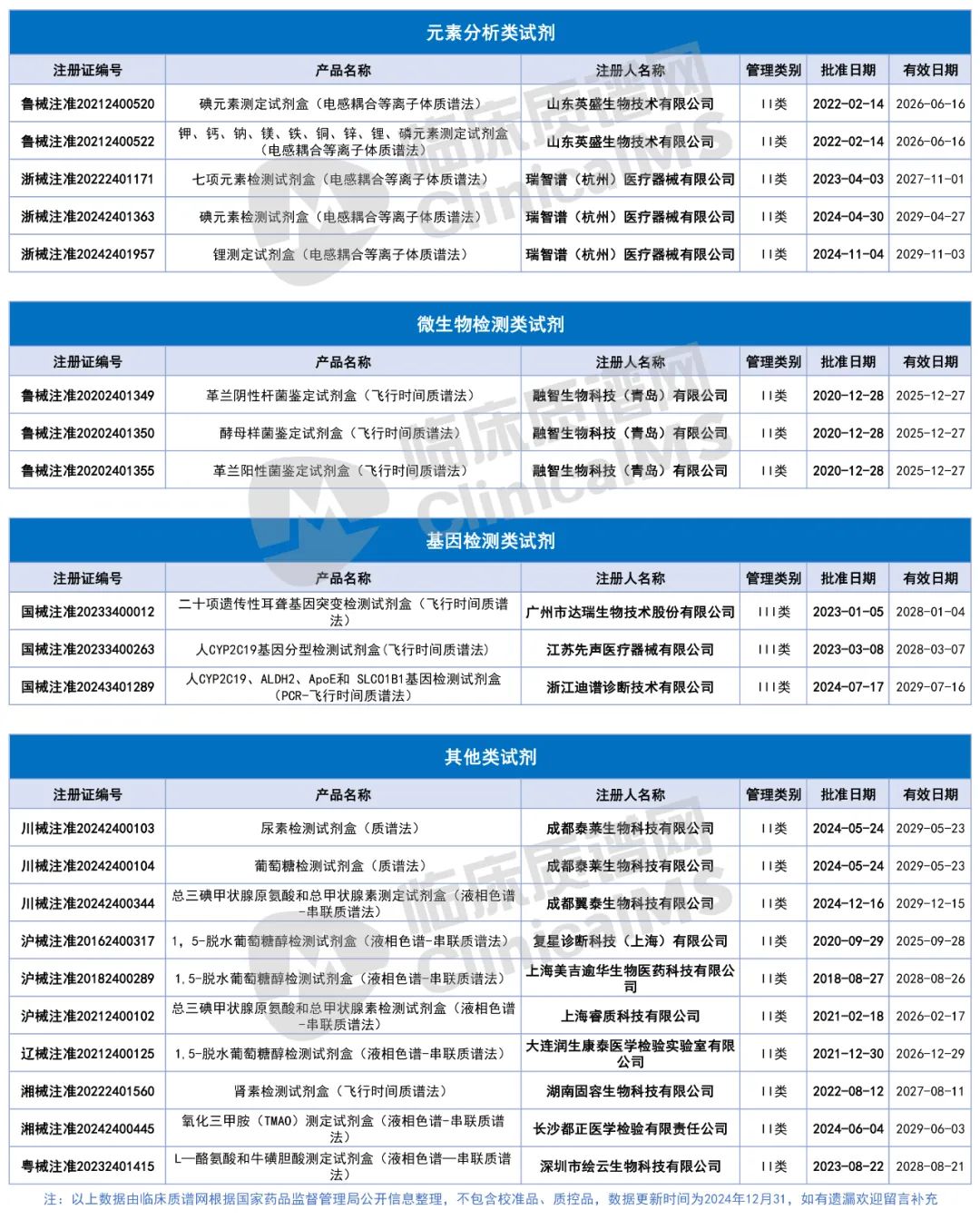
写在最后
在质谱技术的临床应用中,配套的检测试剂与相应耗材发挥着不可或缺的作用。商品化试剂盒一般整合了质谱检测所需的多种物料,涵盖校准品、质控品、样品制备耗材、色谱柱、流动相、数据分析处理软件、说明书等,这些组件或全部包含,或包含其中一部分。
商品化试剂盒具有诸多显著优势,如:医学检测实验室无需自行开发检测项目,极大地节省了时间、人力和物力;其方法学经过系统的性能验证,稳定性和可靠性较高;操作流程说明实现了标准化,便于操作人员使用;减少了实验室对高知识技能的质谱专业人员的依赖。
近年来,国内实验室自建检测(LDT)管理也在加速探索中。2022年12月,国家药监局综合司、国家卫健委办公厅发布了《关于开展医疗机构自行研制使用体外诊断试剂试点的工作通知》;2023年3月,上海市药品监督管理局会同上海市卫生健康委员会制定了《上海市医疗机构自行研制使用体外诊断试剂试点实施方案》。这两个配套支持政策落地实施的文件,分别确定了北京协和医院、上海儿童医学中心、复旦大学中山医院、瑞金医院等10家医院为LDT 试点医院,各省LDT试点政策也在紧锣密鼓的制定当中。2024年7月19日,上海儿童医学中心自行研制体外诊断试剂“五项抗癫痫药物浓度测定试剂盒(液相色谱串联质谱法)”完成备案。该产品是医疗机构自行研制使用体外诊断试剂试点工作开展以来,首个备案的自行研制体外诊断试剂,这也意味着国内LDT政策的正式落地。
随着LDT政策的逐渐落地,质谱配套试剂商品化与LDT将形成“双轮驱动”,协同发力。试剂商品化加速质谱技术普及,LDT 政策激发创新潜能。未来 5 年,伴随更多自研试剂完成备案,国产质谱设备取得突破,中国临床质谱市场有望成为全球精准医疗领域的重要创新力量。















