【冯仁丰】认识临床实验室的溯源性(11):不同计量水平下的实现溯源性的过程(6)
发布日期:2019-11-11 来源:本站 浏览数:4194 人
本微信将继续向大家介绍ISO 17511的征求意见稿中,第六个计量溯源的情况。
即被测量既没有国际认可的参考物质、也无国际认可的参考检测程序,不可溯源至SI。是厂商自行建立的检测方法和控制品。
5.6 被测量仅可溯源至厂商的内部确定的/专利的校准品;没有一级校准品或参考程序;没有溯源性至SI(图6)
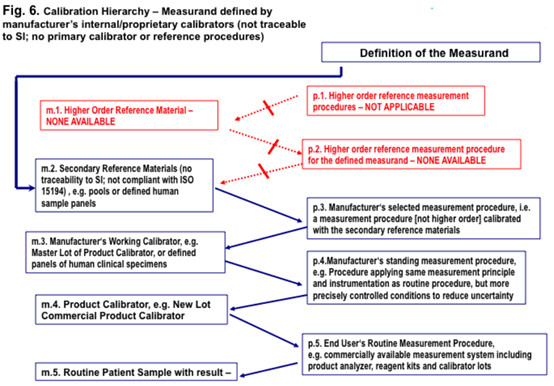
图6、校准层次- 由厂商的内部/专利校准品确定的被测量(没有可溯源至SI;没有一级校准品或参考程序)
5.6.1 一组人的临床样品(m.2),没有可溯源至SI单位,应是二级参考物质,用于校准厂商的选定检测程序(p.3),这不是一个参考检测程序。
注:厂商选定的检测程序会与厂商常设检测程序(p.4)或常规检测程序(p.5)相同,但是要在更紧密的控制条件下实施,以减少被检测量的不确定度。
5.6.2 厂商选定的检测程序(p.3)应是一个检测系统,以二级校准品校准,应被用于确定厂商工作校准品(m.3)的设定值。
注:二级校准品(m.2)会是一组各个人的临床样品,或人的临床样品的混合样品。
5.6.3 厂商这个校准品(m.3)应具由厂商选定检测程序(p.3)为之设定它的值。这个校准品有时被称为“厂商的一级(master)校准品”(或“内部校准品”)。厂商工作校准品(m.3)应已经证明了在厂商选定检测程序(p.3)和厂商常设检测程序(p.4)中有互换性。
注1:厂商负责校准品(m.3)可以是,如具有类似于在终点用户的常规检测程序检测的人原始样品内的基质。
注2:厂商工作校准品可以是一组人的临床样品。
5.6.4 厂商常设的检测程序(p.4)应确定一个检测程序,被一个或更多的厂商工作校准品(m.3)或较高类型的校准品如一组人临床样品(m.2)校准。并确认了分析特异性。
注:厂商常设检测程序会用户常规检测程序(p.5)一样,或可依据相同检测原理和方法,但在更精密的控制条件下实施,以减少检测量的不确定度。
5.6.5 厂商产品校准品(m.4)应按照厂商常设检测程序设定它的值,被预期用于被临床实验室校准使用的常规检测程序。
注1:厂商产品校准品可以是,如具有类似于在终点用户的常规检测程序检测的人原始样品内的基质的物质。
注2:厂商产品校准品,会与人原始的样品是不可互换的,在这个情况下可以设定一个程序特定的校正因子,去纠正不可互换性的大小,使得病人样品得到的量值,按照设定值的方案(p.2),可溯源到一组人临床样品(m.2)。
5.6.6 临床实验室使用的常规检测程序(p.5),应描述为一个检测系统,经常由厂商supply提供,被一个或更多的厂商产品校准品校准。
5.6.7 在一个校准层次的水平(一个校准品和程序对)被取消下,可减少不确定度。见第5.1.3节的限定。
有关这个溯源性内容,可参见前一些时间我为BRAHMS的降钙素原产品溯源性写的微信内容。就是这样的溯源过程。(完)
来源:微信公众号“冯仁丰”

热门推荐
我要留言















