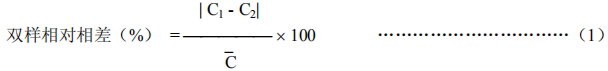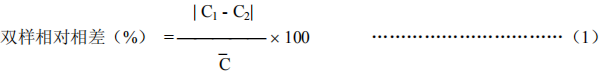前言:本标准规定了血液、尿液、组织及毛发中单乙酰吗啡、吗啡和可待因的免疫筛选法、气相色谱-质谱联用法和液相色谱-串联质谱法测定方法。本站只介绍后两种方法。
第二篇 气相色谱-质谱联用法
7 原理
单乙酰吗啡、吗啡和可待因在约 pH9.2 时可用氯仿:异丙醇(9:1)从生物检材中提出,用丙酸酐使单乙酰吗啡、吗啡和可待因结构上的羟基基团丙酰化后,用气相色谱-质谱联用仪进行检测,经与平行操作的单乙酰吗啡、吗啡或可待因对照品比较,以保留时间和特征碎片离子定性分析。
8 试剂和材料
除另有规定外,试剂均为分析纯,水为 GB/T 6682 规定的二级水。
8.1 单乙酰吗啡、吗啡和可待因对照品
纯度≥99%。
8.2 单乙酰吗啡、吗啡和可待因对照品溶液的制备
分别精密称取对照品单乙酰吗啡、吗啡、可待因各适量,用甲醇配成 1mg/mL 的对照品储备溶液,置于-18ºC 冷冻保存,保存期为 1 年。试验中所用其它浓度的标准溶液均从上述储备液稀释而得,储存在 4℃冰箱中,保存期为 6 个月。
8.3 氯仿。
8.4 异丙醇。
8.5 10%氢氧化钠溶液。
8.6 丙酸酐。
8.7 吡啶。
8.8 硼砂缓冲液
pH9.0~9.2。
8.9 甲醇。
8.10 丙酮。
8.11 0.1%十二烷基磺酸钠溶液。
8.12 0.1%洗洁精溶液。
8.13 浓盐酸。
8.14 0.1mol/L 盐酸溶液。
8.15 MSTFA。
8.16 乙腈。
9 仪器
9.1 气相色谱-质谱联用仪
配有电子轰击源(EI)。
9.2 分析天平
感量0.1mg。
9.3 微波炉。
9.4 涡旋混合器。
9.5 离心机。
9.6 恒温水浴锅。
9.7 空气泵。
9.8 移液器。
9.9 具塞离心试管。
9.10 冷冻研磨机。
10 测定步骤
10.1 样品预处理
10.1.1 尿液直接提取
取尿液 2mL 置于 10mL 具塞离心管中,用 10%氢氧化钠溶液调至 pH 9.0~9.2,加入 1mL硼砂缓冲液,用氯仿:异丙醇(9:1)3mL 提取,涡旋混合、离心,转移有机层至另一离心管中,约 60°C 水浴中空气流下吹干。残留物中加入丙酸酐(50μL)、吡啶(20μL),混匀,微波炉(500W)衍生化 3min,60°C 水浴中空气流下吹干,残留物用 30μL 甲醇溶解,取 1μL 进气相色谱-质谱联用仪分析。
10.1.2 尿液中总吗啡或可待因的提取
取尿液 2mL 置于 10mL 具塞离心管中,加入 0.2mL 浓盐酸沸水浴中水解 30min,取出,冷却后加入 1mL 正丁醇,涡旋混合、离心,弃去有机层,用 10% 氢氧化钠溶液调至 pH 9.0~9.2,以下同 10.1.1 项下操作。
10.1.3 血液直接提取
取血液 2mL 置于 10mL 具塞离心管中,加入 2mL 硼砂缓冲液,用氯仿:异丙醇(9:1)3mL提取,以下同 10.1.1 项下操作。
10.1.4 组织提取
将组织剪碎或匀浆,称取 2g,加入 2mL 水,再加入 0.4mL 浓盐酸,沸水浴中水解 30min,取出,用 10%氢氧化钠溶液调至 pH 9.0~9.2,以下同 10.1.1 项下操作。
10.1.5 毛发提取
10.1.5.1 毛发采集
贴发根处剪取毛发,发根处作标记。
10.1.5.2 毛发洗涤
毛发样品依次用 0.1%十二烷基磺酸钠溶液、0.1%洗洁精溶液、水和丙酮振荡洗涤一次,晾干后剪成约 1mm 段,供检。
10.1.5.3 毛发的提取、净化
称取 50mg 毛发,加 1mL 0.1mol/L 盐酸溶液浸润,45°C 水浴水解 12~15 小时或超声 1小时(针对磨碎的头发),取出后用 10%氢氧化钠溶液调至 pH 9.0~9.2,加入 1mL 硼砂缓冲液,,用氯仿:异丙醇(9:1)3mL 提取,涡旋混合、离心,转移有机层至另一离心管中,约 60°C水浴中空气流下吹干。残留物中加入 MSTFA(25μL)、乙腈(25μL),混匀,微波炉(500W)衍生化 3min,冷却后取 1μL 进气相色谱-质谱联用仪分析。
10.2 样品测定
10.2.1 气相色谱-质谱参考条件
a) 色谱柱:HP-1MS 毛细管柱(30m×0.25mm×0.25μm)或相当者;
b) 柱温:100°C 保持 1.5min,以 25°C/min 程序升温至 280°C,保持 15min;
c) 载气:氦气,纯度≥99.999%,流速:1.0mL/min;
d) 进样口温度:250°C;
e) 进样量:1μL;
f) 电子轰击源:70eV;
g) 四极杆温度:150°C;
h) 离子源温度:230°C;
i) 接口温度:280°C;
j) 检测方式:SIM。
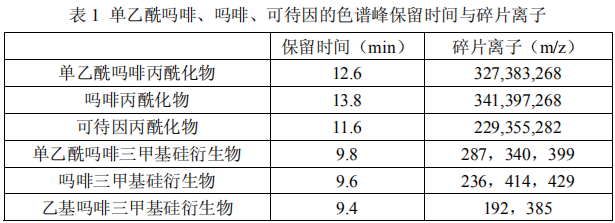
每种化合物分别选择 3 个特征碎片离子。单乙酰吗啡、吗啡、可待因的保留时间与特征碎片离子见表 1。
10.2.2 定性测定
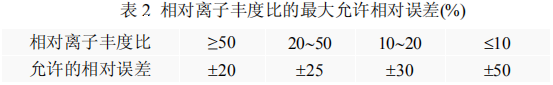
进行样品测定时,如果检出的色谱峰保留时间与空白检材添加对照品的色谱峰保留时间比较,相对误差小于 2%,并且在扣除背景后的样品质谱图中,所选择的离子均出现,而且所选择的离子相对丰度比与添加对照品的离子相对丰度比之相对误差不超过表 2 规定的范围,则可判断样品中存在这种化合物。
10.2.3 定量测定
采用外标-校准曲线法或单点法定量。用相同基质空白添加适量目标物对照品制得一系列校准样品,以目标物的峰面积对目标物浓度绘制校准曲线,并且保证所测样品中目标物的浓度值在其线性范围内。当检材中目标物浓度在空白检材中添加目标物浓度的±50% 以内时,可采用单点校准法来计算目标化合物的浓度。
10.3 平行试验
样品应按以上步骤同时平行测定两份。
平行试验中两份检材测定结果按两份检材的平均值计算,双样相对相差不得超过 20%(腐败检材不超过 30%)。双样相对相差按式(1)计算:
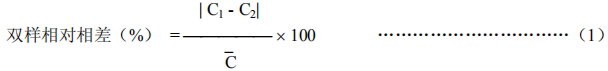
式中:
C1、C2 ⎯⎯两份样品平行定量测定的结果;
`C ⎯⎯两份样品平行定量测定结果的平均值(C1+ C2)/ 2。
10.4 空白试验
除以相同基质空白替代检材外,均按上述步骤进行。
11 结果计算
以外标-校准曲线法或按式(2)计算被测样品中单乙酰吗啡、吗啡或可待因浓度:

式中:
C ⎯⎯检材中目标物的浓度(μg/mL 或μg/g)
A1 ⎯⎯检材中目标物的峰面积
A2 ⎯⎯空白检材中添加目标物的峰面积
W ⎯⎯空白检材中目标物的添加量(μg)
W1 ⎯⎯检材量(mL 或 g)
12 方法检出限
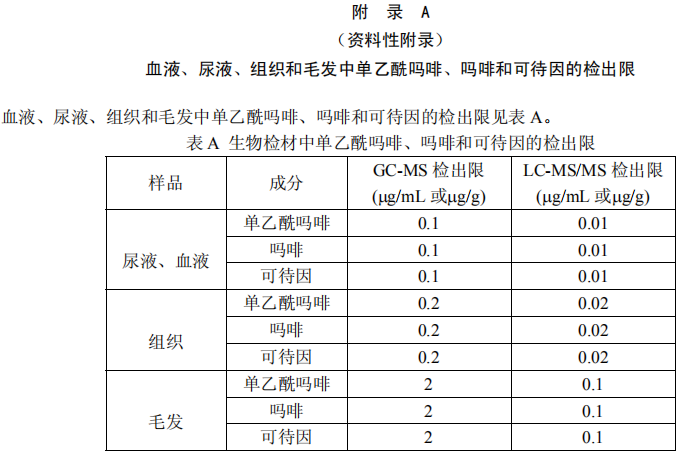
血液、尿液、组织和毛发中单乙酰吗啡、吗啡和可待因的检出限见附录A。
第三篇 液相色谱-串联质谱法
13 原理
单乙酰吗啡、吗啡、可待因在约 pH9.2 时可用氯仿:异丙醇(9:1)从生物检材中提出,提取后的样品用液相色谱-串联质谱法的多反应监测模式进行检测,经与平行操作的单乙酰吗啡、吗啡和可待因对照品比较,以保留时间和两对母离子/子离子对进行定性分析。
14 试剂和材料
除另有规定外,试剂均为分析纯,水为 GB/T 6682 规定的一级水。
14.1 单乙酰吗啡、吗啡、可待因对照品及溶液的制备
同 8.1 及 8.2。
14.2 氯仿。
14.3 异丙醇。
14.4 丙酮。
14.5 硼砂缓冲液
pH 9.0~9.2。
14.6 浓盐酸。
14.7 0.1mol/L 盐酸溶液。
14.8 10%氢氧化钠溶液。
14.9 0.1%十二烷基磺酸钠溶液。
14.10 0.1%洗洁精溶液。
14.11 乙腈
色谱纯。
14.12 甲酸
优级纯。
14.13 乙酸胺
色谱纯。
14.14 流动相缓冲液
20mmol/L 乙酸铵和 0.1%甲酸缓冲液:分别称取 1.54g 乙酸铵和 1.84g 甲酸置于 1000mL容量瓶中,加水定容至刻度,pH 值约为 4。
15 仪器
15.1 液相色谱-串联质谱仪
配有电喷雾离子源(ESI)。
15.2 分析天平
感量0.1mg。
15.3 涡旋混合器。
15.4 离心机。
15.5 恒温水浴锅。
15.6 空气泵。
15.7 移液器。
15.8 具塞离心试管。
15.9 冷冻研磨机。
16 测定步骤
16.1 样品预处理
16.1.1 尿液提取
取尿液 2mL 置于 10mL 具塞离心管中,用 10%氢氧化钠溶液调至 pH 9.0~9.2,加入 1mL硼砂缓冲液,用氯仿:异丙醇(9:1)3mL 提取,涡旋混合、离心,转移有机层至另一离心管中,约 60°C 水浴中空气流下吹干。残留物中加入 100μL 乙腈:流动相缓冲液(70:30)进行溶解,取5μL 进 LC-MS/MS。
16.1.2 血液提取
取血液 2mL 置于 10mL 具塞离心管中,加入 2mL 硼砂缓冲液,用氯仿:异丙醇(9:1)3mL提取,以下同 15.1.1 项下操作。
16.1.3 组织提取
将组织剪碎或匀浆,称取 2g,加入 2mL 水,再加入 0.4mL 浓盐酸沸水浴中水解 30min,取出,用 10%氢氧化钠溶液调至 pH9.0~9.2,以下同 15.1.1 项下操作。
16.1.4 毛发提取
称取 50mg 毛发,加 1mL 0.1mol/L 盐酸溶液浸润,45°C 水浴水解 12~15 小时或超声 1小时(针对磨碎的头发),取出后用 10% 氢氧化钠溶液调至 pH9.0~9.2,加入 1mL 硼砂缓冲液,以下同 15.1.1 项下操作。
16.2 样品测定
16.2.1 液相色谱-串联质谱参考条件
a) 色谱柱:Allure PFP Propyl 100mm×2.1mm×5μm 或相当者,前接保护柱;
b) 柱温:室温;
c) 流动相:V(乙腈) : V(缓冲液) = 70 : 30;
d) 流速:200μL/min;
e) 进样量:5μL;
f) 扫描方式:正离子扫描(ESI+);
g) 检测方式:多反应监测(MRM);
h) 离子喷雾电压:5500 V;
i) 离子源温度:500°C;
j) 每个化合物分别选择 2 对母离子/子离子对作为定性离子对,以第一对离子对作为定量离子对。其定性离子对、定量离子对、去簇电压(DP)、碰撞能量(CE)和保留时间(tR)见表3。
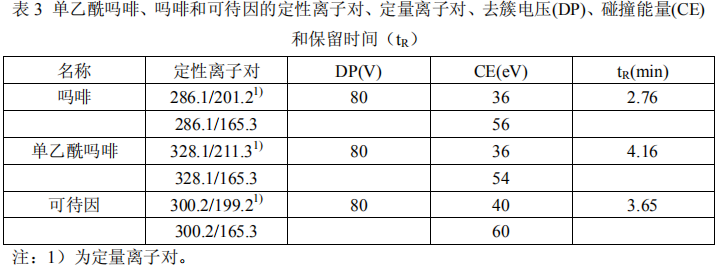
16.2.2 定性测定
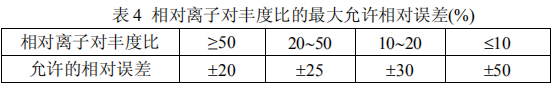
进行样品测定时,如果检出的色谱峰保留时间与空白检材添加对照品的色谱峰保留时间比较,相对误差小于 2%,并且在扣除背景后的样品质谱图中,均出现所选择的离子对,而且所选择的离子对相对丰度比与添加对照品的离子对相对丰度比之相对误差不超过表 4 规定的范围,则可判断样品中存在这种化合物。
16.2.3 定量测定
采用外标-校准曲线法或单点法定量。用相同基质空白添加适量目标物对照品制得一系列校准样品,以目标物的峰面积对目标物浓度绘制校准曲线,并且保证所测样品中目标物的浓度值在其线性范围内。当检材中目标物浓度在空白检材中添加目标物浓度的±50% 以内时,可采用单点校准法来计算目标化合物的浓度。
16.3 平行试验
样品应按以上步骤同时平行测定两份。
平行试验中两份检材测定结果按两份检材的平均值计算,双样相对相差不得超过 20%(腐败检材不超过 30%)。双样相对相差按式(1)计算:
式中:
C1、C2 ⎯⎯两份样品平行定量测定的结果;
`C ⎯⎯两份样品平行定量测定结果的平均值(C1+ C2)/ 2。
16.4 空白试验
除以相同基质空白替代检材外,均按上述步骤进行。
17 结果计算
以外标-校准曲线法或按式(2)计算被测样品中单乙酰吗啡、吗啡或可待因浓度:
式中:
C ⎯⎯检材中目标物的浓度(μg/mL 或μg/g)
A1 ⎯⎯检材中目标物的峰面积
A2 ⎯⎯空白检材中添加目标物的峰面积
W ⎯⎯空白检材中目标物的添加量(μg)
W1 ⎯⎯检材量(mL 或 g)
18 方法检出限
血液、尿液、组织和毛发中单乙酰吗啡、吗啡和可待因的检出限见附录A。
如需原件,可在下方留言并附上邮箱,我们将会邮件发送!
来源:司法部,如有侵权,请联系删除!