摘 要
液相色谱-串联质谱(LC-MS/MS)在人体血清(浆)类固醇激素检测中展现出优于传统免疫学方法的特异性高、分析测量范围宽、多标志物同时检测等特点,已成为国际内分泌学领域相关疾病实验室诊断的首选方法。目前,国内医学实验室开展血清(浆)类固醇激素LC-MS/MS检测多参考已发表学术论文和仪器厂家说明书提供的通用操作和检测程序。然而,血清(浆)类固醇激素LC-MS/MS检测的技术难度大,临床实验室检验人员大多数缺少质谱领域专业培训和实践经验,而通用程序缺乏针对性和实操性,尤其我国尚无针对该检测程序和质量保证的系统性文件,导致实验室间检测结果存在较大差异,阻碍了该技术的临床应用。为规范我国血清(浆)类固醇激素LC-MS/MS检测,共识从检验前、中、后程序及其质量保证进行详细说明,并提出针对性建议,为实验室开展该检测项目提供参考,以推动我国血清(浆)类固醇激素LC-MS/MS检测的临床应用和结果一致性。
尽管已有众多研究报道多种类固醇激素的LC-MS/MS检测,包括方法开发和优化、生物参考区间建立等,国外已有针对血清(浆)雄激素、雌激素LC-MS/MS检测程序的指南,国内有LC-MS/MS临床应用通用建议共识及25羟-维生素D和雄激素LC-MS/MS检测的共识,但依然缺乏涵盖检验前、中、后阶段的LC-MS/MS检测操作程序和质量保证的指南和共识。基于此,为规范我国血清(浆)类固醇激素LC-MS/MS检测,中国质谱学会临床质谱专家委员会组织专家参阅国内外相关文献并结合临床应用经验,面向医学实验室临床质谱检验人员,针对肾上腺皮质激素和性激素LC-MS/MS分析全流程的质量保证进行详细说明并提出建议,为实验室开展血清(浆)类固醇激素检测项目提供参考,以推动我国血清(浆)类固醇激素检测的临床应用和结果一致性,提升我国类固醇激素异常相关疾病的精准诊断能力。
一、血清(浆)类固醇激素LC-MS/MS检验前质量保证
(一)标本采集
人体类固醇激素浓度受多种因素影响,包括昼夜节律、生理周期、采血体位和药物等,应根据临床具体需求和激素水平影响因素,制定合理采样流程,并推荐给标本采集人员和患者。例如:皮质醇分泌通常在清晨6:00—8:00达到峰值浓度,因此峰值监测推荐清晨采集患者血液标本;连续监测则采样时间点应相对固定;醛固酮仰卧位采血比直立位采血检测结果低50% ;女性患者进行血清(浆)雌激素检测时需明确卵泡期、黄体期等信息,对于无规律月经周期女性,需明确绝经(特别是早绝经)原因,如自然绝经、外科手术、辐射、药物作用等。
含有分离胶的促凝管中存在睾酮干扰峰,且分离胶可吸收类固醇激素,标本体积和储存时间也可不同程度影响检测结果。新生儿CAH二级筛查中,EDTA采血管可导致17α-羟孕酮、雄烯二酮及11-脱氧皮质醇的LC-MS/MS检测结果偏高,造成假阳性 。另外,更换采血管品牌或批号也可能影响待测物色谱峰分离度,应制定包括峰分离度、保留时间漂移范围等色谱参数的可接受标准,以监测潜在干扰峰的影响强弱及变化。
建议1 针对有昼夜和/或周期节律的类固醇激素,实验室应根据其临床预期用途,指导患者和采血人员选择合适的采血时机,例如清晨采血检测皮质醇、睾酮水平,卵泡期采血检测雌激素水平。推荐采用不含分离胶的血清(浆)采血管采集标本,新生儿二级CAH筛查推荐采用肝素抗凝剂采血管。
(二)标本保存和运输
实验室应根据类固醇激素质谱检测的标本保存条件及检测频率进行标本的稳定性验证。标本稳定性验证实验应至少包括环境温度、冷藏和/或冷冻条件下的稳定性,如果标本存在冻存后复查的可能,还需考察反复冻融对标本稳定性的影响。另外,标本采集、运输及前处理阶段的稳定性也需进行评估。标本稳定性实验均需使用新鲜血清(浆),通过比较新鲜采集和保存后的血清(浆)标本检测结果评估其稳定性。
如果实验室根据参考文献报道或试剂说明书设置标本保存条件,需包含明确的稳定性、标本类型、类固醇激素浓度、保存温度范围、保存时间以及保存后标本浓度较新鲜标本的变化百分比。为确保标本保存后类固醇激素检测结果“稳定”或“无明显变化”,需明确测量程序、含量计算程序及含量变化的可接受范围。如果这些信息缺失,实验室应自行建立标本稳定性的可接受条件。
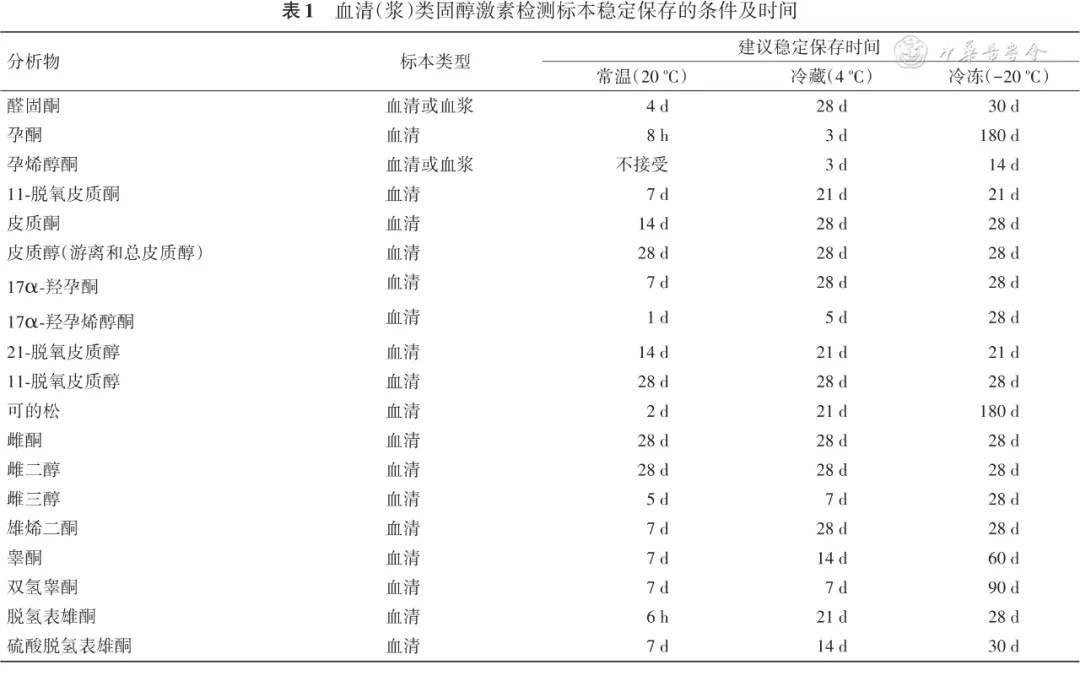
建议2 实验室应根据标本保存的实际需求,使用新鲜标本对来自文献报道或试剂说明书的标本稳定性进行验证,或自建稳定性可接受的标本保存条件。建议血清(浆)标本中类固醇激素稳定保存的条件及时间见 表1 。
二、血清(浆)类固醇激素LC-MS/MS检验质量保证
(一)标本前处理
标本前处理方法取决于待测物的理化性质、灵敏度要求和分析方法。其目的是将待测物从血清(浆)及其他潜在干扰物质中分离、提取、纯化,并实现对待测物的浓缩。大多数糖皮质激素(如17α-羟孕烯醇酮、17α-羟孕酮、11-脱氧皮质醇、皮质醇、可的松)和盐皮质激素(如孕烯醇酮、孕酮、脱氧皮质酮、皮质酮)为疏水结构,均可与相应转运蛋白结合存在于血液中,游离形式约占1%。但血液中,约50%醛固酮以游离形式存在。睾酮和雌二醇与白蛋白结合力弱,与性激素结合球蛋白(sex hormone binding globulin,SHBG)结合力强,2%~4%睾酮呈游离形式,60%~75%睾酮与SHBG结合,20%~40%睾酮与白蛋白结合。平衡透析可去除血中结合型类固醇激素进而检测游离型激素水平,但测量程序要求更高的灵敏度。如果结合型类固醇在水解前无法被直接检测,则需水解后进行检测,并明确结合型类固醇是否完全水解,且水解步骤不会导致类固醇降解,如硫酸雌酮在提取之前需通过水解酶获得游离型雌酮。亲脂性性激素(雄烯二酮、睾酮、双氢睾酮、雌酮、雌二醇、雌三醇)较亲水性性激素(硫酸脱氢表雄酮、硫酸雌酮)在血液中浓度低,因此亲脂性性激素的LC-MS/MS测量程序通常需要更复杂的标本前处理以消除基质干扰并浓缩待测物以达到理想的定量限(limit of quantification,LOQ)。
血清(浆)类固醇激素LC-MS/MS检测的标本前处理流程通常包括:(1)取等量临床标本、标准品、质控品和基质空白;(2)加入内标物;(3)提取;(4)纯化。对易氧化的类固醇激素,前处理时需尽可能避免发生氧化以防待测物降解及产生干扰物。例如,在样品浓缩时使用惰性气体(如氮气),而非加热真空离心浓缩。去除可能干扰检测或影响前处理的物质后,宜将分析物转移到液相色谱流动相洗脱溶剂中,保持初始浓度比例,以备后续分析。推荐使用与待测物具有相似结构和离子化性质的同位素标记物(或结构类似物)作为类固醇激素LC-MS/MS检测内标物,例如氘代或 13C标记的类固醇。通过比较已知浓度内标物与待测物的信号,校正样本前处理、色谱分离、离子化过程及基质效应所产生的误差。类固醇激素的同位素内标物大多为商品化试剂,如无商品化试剂,应优先选择使用非内源性但与待测物结构类似的合成类固醇作为内标物,并确保内标物与待测物具有相同或相近保留时间。内标物的相对分子质量应至少比相应待测物大3,氘代或 13C标记数量控制在7,化学纯度应≥98%,同位素内标物纯度≥97%。
内标物需加入到所有校准品、质控品和待测标本中,且应在提取或纯化步骤之前或同时加入。加入内标物后需静置足够长的时间(通常15~30 min)以平衡内标物与结合蛋白的相互作用,抵消因蛋白结合导致的检测浓度偏低,如睾酮和睾酮-d 3需30 min完成平衡(22 ℃)。内标物的质谱信号强度应在不同分析批次中保持稳定,平衡时间不足可能会导致内标物信号强度不稳定。
建议3 使用与待测物有相同理化性质的商品化同位素标记物作为类固醇激素LC-MS/MS检测内标物( 表2 ),浓度设置在校准曲线的中浓度或医学决定水平附近,实验室应制定内标物信号强度波动的批间可接受范围。

血液中存在的大量蛋白质、多肽、小分子化合物等可引起LC-MS/MS的离子源和检测器饱和,导致离子抑制或分辨率不足,干扰检测结果。因此,LC-MS/MS分析前应提取待检测物,去除无机化合物(如盐)、蛋白质、脂质(如甘油三酯)和磷脂等物质的干扰,提高检测灵敏度、重复性和稳定性。
LC-MS/MS分析标本的提取方法包括蛋白沉淀(protein precipitation,PPT)、液液萃取(liquid-liquid extraction,LLE)、固相萃取(solid-phase extraction,SPE)等。PPT利用蛋白沉淀剂使蛋白变性沉淀,离心后直接取上清液进行检测,不适用于含量较低或有蛋白结合特性的类固醇激素。LLE利用溶剂的相似相溶原理,将目标化合物从液体混合物中分离出来,因操作繁琐且需要消耗大量有机溶剂,故临床常用固相支撑液液萃取(supported liquid extraction,SLE)替代传统LLE,降低有机溶剂消耗。而SPE采用固体颗粒色谱填料(通常填充于小柱型装置中)对样品不同组分进行化学分离,较SLE具有更优的去磷脂干扰能力,是类固醇激素标本提取的首选方法,但也具有操作步骤多、成本高等缺点。针对类固醇激素的不同极性,脂溶性激素通常选择亲脂基团填料的SPE方法萃取待测物,非脂溶性激素选择亲水基团或阴阳离子交换填料的SPE方法萃取待测物。为进一步去除与待测物共同洗脱的干扰物,可联合LLE和SPE,或吹干提取物后用不同溶剂重新提取。其中,通过高效液相色谱(high performance liquid chromatography,HPLC)可在线进行SPE,以减少手工操作,节省时间和人力成本,但目前尚无多种类固醇激素在线SPE提取解决方案。也有通过使用单个或多个提取柱串联色谱柱,如提取/上样柱、一次性SPE柱、二维色谱,提高色谱分离效率和检测灵敏度,使血清(浆)标本无需或只需经简单蛋白沉淀处理即可进行分析。
建议4 根据待测类固醇激素理化性质及测量灵敏度要求推荐使用SLE或SPE标本提取方法。
(二)类固醇激素LC-MS/MS定量分析
LC-MS/MS通过结合HPLC的高效分离浓缩能力与三重四极杆质谱的高特异性和高灵敏度定量性能,准确测量标本中浓度极低、理化性质相似的类固醇激素,其特异性较免疫学分析明显提高。
1. HPLC分离
HPLC是一种基于待测物在固定相和流动相中具有不同分配系数的分离技术。通常使用对非极性分子具有高亲和力的非极性固定相(如 18C、五氟苯基等)色谱柱分离类固醇激素,通过流动相极性变化将吸附于色谱柱上的类固醇激素重新溶于流动相,从而实现逐步洗脱分离。通过开发精密的流动相梯度洗脱程序和使用适合的色谱柱可以分离结构非常相似的类固醇激素及其代谢物,包括一些同分异构体(如21-脱氧皮质醇、11-脱氧皮质醇)。通过依次洗脱标本中所有待测物,降低检测信号的复杂度,分离组分信号随时间出现一组近似高斯分布的色谱峰群,生成检测信号强度随时间变化的色谱图。另外,流动相中通常加入挥发性添加剂(如0.01 mol/L甲酸铵、0.1%甲酸),其浓度不应超过0.5%,以增强化合物离子化,而不应含非挥发性流动相添加剂。色谱柱可选择粒径较小的分离柱,实现短时间内更好的分离效果,也可根据文献综合选择。色谱柱应在寿命期限内使用,并根据检测量、峰型、保留时间、分离度、柱压等参数判断是否需要更换。实验室应做好色谱柱的日常维护,在每日检测结束后进行日常冲洗程序,并最终将色谱柱保持在95%及以上的甲醇或乙腈中,尽可能地延长色谱柱的使用寿命及使用质量。
建议5 为有效分离结构相似的类固醇激素及其代谢产物,推荐实验室使用 18C或五氟苯基填料,色谱柱粒径≤3 μm,有机相梯度洗脱程序:0.5~4.0 min,40%~55%;4.0~6.5 min,55%~75%;6.5~7.5 min,75%~99%。
2. 串联质谱检测
类固醇激素LC-MS/MS测量程序使用的离子源主要包括电喷雾电离(electrospray ionization,ESI)和大气压化学电离(atmospheric pressure chemical ionization,APCI)。在常规临床检测中,醛固酮、皮质醇、11-脱氧皮质醇、21-脱氧皮质醇、可的松、睾酮、孕酮、17α-羟孕酮、皮质酮、雄烯二酮、脱氢表雄酮可采用ESI或APCI离子源。与ESI相比,APCI离子源温度更高,脱溶剂更充分,因此基质效应更小。然而,APCI更适用极性较小的类固醇激素,如3β-羟基-5-烯类固醇 ,在需同时检测多个类固醇激素的临床应用中具有局限性。
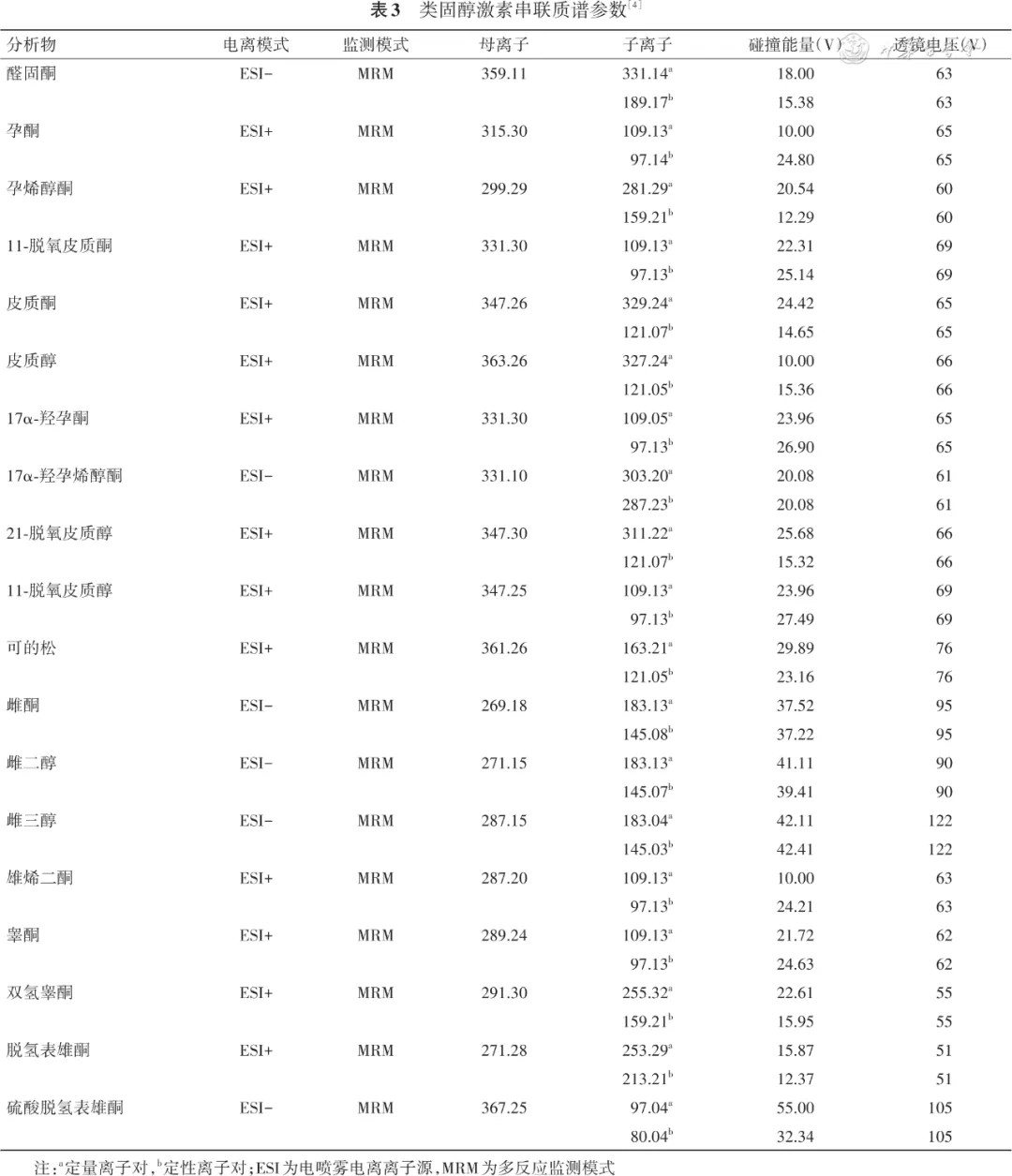
类固醇激素分子经离子源电离后进入三重四极杆质量分析器,根据质荷比进行分离,并采用多反应监测(multiple reaction monitoring,MRM)或选择反应监测(selected reaction monitoring,SRM)模式采集数据。最终借助质量分析器选择特定母离子和子离子,通过母离子/子离子对和各分析物及内标物的色谱图及峰面积对目标化合物进行定量。不同仪器,其离子对信息及检测参数并不完全相同,每个化合物通常选择2个离子通道分别作为定性离子和定量离子通道( 表3 )。基于定性离子、化合物极性及内标物分离峰综合判断目标化合物的分离峰。
建议6 类固醇激素LC-MS/MS检测选择ESI或APCI离子源,采用MRM或SRM模式,应在性能验证时优化质谱参数。
3. LC-MS/MS测量程序性能验证和/或确认
测量程序的性能要求取决于其预期临床用途、待测类固醇激素生物学变异及仪器灵敏度水平。如检测女性、儿童血清睾酮,测量程序的灵敏度需要达到0.02 ng/ml;同时检测浓度差异大的多个分析物,如雌二醇、雌酮、雄烯二酮,需验证测量程序对每个分析物的分析性能是否满足临床需求。值得注意的是,由于血清(浆)类固醇激素LC-MS/MS测量程序包含的人工操作步骤多,各实验室环境条件、仪器设备配置、人员水平相差大,因此即使实验室使用商品化试剂盒(Ⅰ、Ⅱ类),也应进行性能确认或验证。LC-MS/MS测量程序性能验证和/或确认程序可参考共识或美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)C62-A,并根据生物变异、临床指南、政策法规等设定性能验证中每项参数的可接受标准。
(三)类固醇激素LC-MS/MS测量程序的分析性能指标
类固醇激素相关疾病的临床诊断对检测指标及灵敏度有不同需求,实验室应综合临床需求及仪器灵敏度确定LC-MS/MS测量程序分析性能。
1.肾上腺皮质激素
皮质醇是最主要的肾上腺皮质激素(约占75%~95%),血液中总皮质醇、游离皮质醇水平及昼夜节律变化常用于辅助诊断原发性和继发性肾上腺功能不全、库欣综合征、艾迪生病。正常成人清晨血清总皮质醇浓度通常在20~50 ng/ml,经平衡透析后的游离皮质醇浓度约占总皮质醇5%,可更准确反应皮质醇水平及节律,推荐检测血清(浆)游离皮质醇(LOQ≤1 ng/ml)。皮质醇联合17α-羟孕酮、雄烯二酮常用于筛查11-羟化酶或21-羟化酶缺乏型CAH。大多数(约90%)CAH由21-羟化酶基因变异导致,患者血清雄烯二酮水平通常升高5~10倍,17α-羟孕酮水平升高幅度更大,而皮质醇水平较低或无法检测。不同年龄、性别人群17α-羟孕酮及雄烯二酮水平差异较大,推荐实验室检测17α-羟孕酮(LOQ≤0.1 ng/ml),检测区间上限设定在参考区间上限10倍以上。
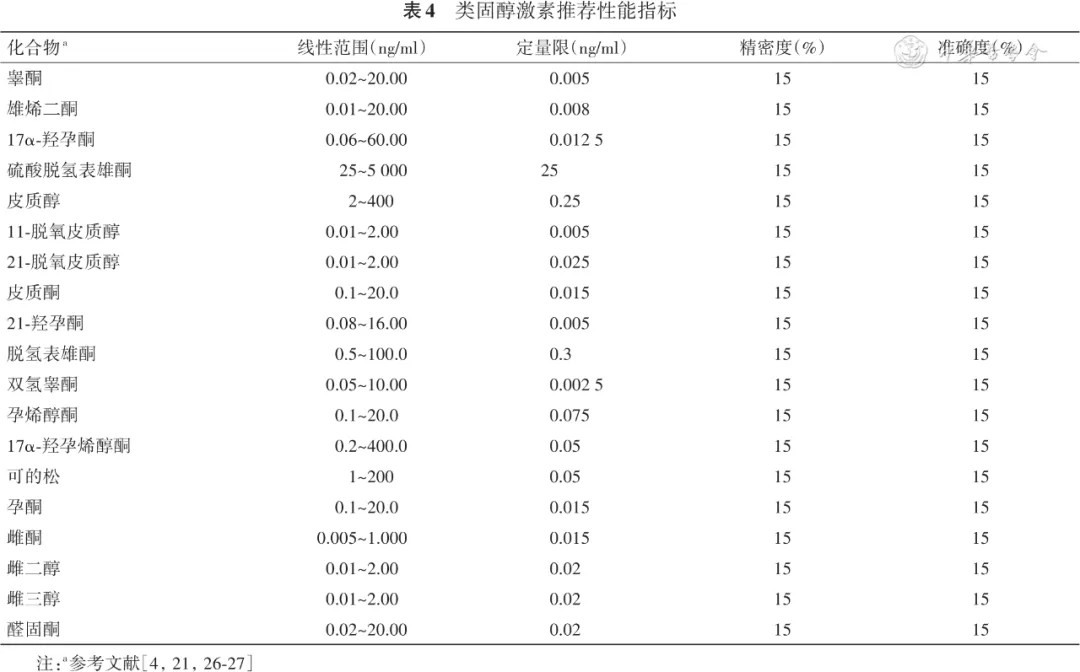
硫酸脱氢表雄酮、孕烯醇酮、孕酮、17α-羟孕烯醇酮、11-脱氧皮质酮和18-羟皮质酮常用于已排除11-羟化酶、21-羟化酶缺乏型CAH,及确认3β-羟基类固醇脱氢酶缺乏和17α-羟化酶缺乏型CAH。在非常罕见的17α-羟化酶缺乏症中,雄烯二酮、所有雄激素前体(17α-羟孕烯醇酮、17α-羟孕酮、硫酸脱氢表雄酮)、睾酮、雌酮、雌二醇和皮质醇水平降低,而盐皮质激素(孕酮、11-脱氧皮质酮和18-羟皮质酮)水平明显升高。醛固酮是典型的盐皮质激素,常用于辅助诊断原发性醛固酮增多症(如肾上腺肿瘤、肾上腺皮质增生)和继发性醛固酮增多症(如肾血管疾病、盐耗竭、钾负荷、肝硬化腹水、心力衰竭、妊娠、Bartter综合征),以上情况醛固酮水平通常可升高10~100倍。因此,建议醛固酮LOQ≤0.02 ng/ml,检测区间上限设定在参考区间上限100倍( 表4 )。
2.雄激素
LC-MS/MS较易检测正常成年男性雄激素水平,但对低雄激素水平人群,如女性、儿童以及性腺功能减退的男性,则要求测量程序具有更高的灵敏度。对成年女性,睾酮水平通常用于评估由肾上腺合成异常和PCOS导致的高雄激素血症及相关的女性多毛症、月经紊乱、不孕等疾病。对儿童,睾酮水平通常用于评估外生殖器性别模糊、性早熟或发育延迟,以及用于CAH的诊断。建议女性或儿童的睾酮测量程序LOQ≤0.02 ng/ml,并需配置高灵敏度LC-MS/MS系统,并对样品进行离线或在线前处理,如LLE、SPE或多个提取步骤结合(如PPT结合SPE) 。
双氢睾酮以及双氢睾酮/睾酮比值可用于诊断雄激素缺乏症、监测雄激素替代治疗或5α-还原酶抑制剂疗效,建议采用双氢睾酮非衍生化法LC-MS/MS检测(LOQ≤0.05 ng/ml)。雄烯二酮还可用于诊断和评估女性高雄激素血症、多毛症、不孕症,儿童性早熟、发育延迟、CAH,以及肾上腺、性腺肿瘤。在CAH、女性高雄激素血症等疾病中,雄烯二酮水平明显升高,但在3β-羟基类固醇脱氢酶缺乏症、17α-羟化酶缺乏症及类固醇合成急性调节蛋白缺乏症等罕见病及2岁以下儿童中,其水平较正常成人明显降低,建议其LOQ≤0.02 ng/ml。雄烯二酮检测的子离子与睾酮子离子具有相同的质荷比,因此实验室需验证睾酮和雄烯二酮的色谱分离度。
脱氢表雄酮和硫酸脱氢表雄酮除联合肾上腺皮质激素用于CAH辅助诊断以外,还可用于鉴别诊断肾上腺功能不全或亢进。与性激素联合可用于区分肾上腺功能初现与性早熟,诊断儿童CAH和女性PCOS。儿童脱氢表雄酮水平较低(通常1~8岁儿童<2 ng/ml),为了准确诊断儿童肾上腺功能初现、性早熟,建议脱氢表雄酮LOQ≤0.02 ng/ml,硫酸脱氢表雄酮LOQ≤30 ng/ml。
3.雌激素
对低浓度雌激素的准确检测可用于儿童性发育延迟或性早熟的评估,以及绝经后女性乳腺癌发病风险或芳香酶抑制剂治疗效果评估。非衍生化前处理,ESI负离子模式下检测雌二醇、雌酮及雌三醇建议LOQ≤0.01 ng/ml。硫酸雌酮在体内的浓度是雌二醇和雌酮的10~50倍,且半衰期较长,因此可用于雌激素水平状况评估。
建议7 实验室应根据临床需求、待测类固醇激素生物学变异及仪器灵敏度水平,建立分析性能满足要求的类固醇激素LC-MS/MS测量程序( 表4 )。
(四)类固醇激素LC-MS/MS测量程序的质量保证
1. 量值溯源
量值溯源是通过一条具有明确不确定度的不间断传递链,使测量结果的量值能够与规定的参考标准(国家或国际计量标准)联系起来 。类固醇激素量值的可溯源性是实现实验室间测量结果一致的基础,即同一标本在不同时间和地点采用不同测量程序得到准确测量结果。实验室应参考国际标准化组织(International Organization for Standardization,ISO)17511文件及中国合格评定国家认可委员会关于测量结果的计量溯源性文件要求建立计量溯源链,核心要素包括被测物、参考物质、校准及赋值程序、测量结果验证 。
实验室应参考国际临床化学和检验医学联合会/国际纯粹与应用化学联合会文件明确被测物属性,包括分析物特性(如化学形式)、测量基质、单位等;可通过检验医学溯源联合委员会网站或国家标准物质资源共享平台查询参考物质信息,并优先选择具有明确溯源信息的参考物质(如有证参考物质)作为校准品。对无有证参考物质的类固醇激素,实验室应参考CLSI EP30评估校准品的特性、纯度、均一性、稳定性及互通性并制定相关评估程序。
需明确的是,计量溯源链本身并不直接保证测量结果的准确性和一致性,溯源链中每次量值传递都会新增测量不确定度,测量的准确度和不确定度也可能在使用新校准品或仪器大修后改变,实验室应通过检测校准品、参加能力验证计划或实验室间比对,明确测量程序的正确度和精密度。
建议8 实验室应优先选择具有明确溯源信息的类固醇激素参考物质作为校准品,建立计量溯源链。
2. 校准
校准是确定或校正质谱仪检测信号强度与待测物浓度之间的相关性。通常将校准物质加入到经活性炭处理、不含待测类固醇激素的单一来源或混合血清(浆)基质中以制备一系列稀释校准品。类固醇激素LC-MS/MS测量程序性能验证、更换试剂或校准物批号后,需确定每个分析批校准曲线的斜率、截距和相关系数的可接受标准。每个分析批都需进行校准,如果一个分析批包含的样品很多,校准品可在分析批不同位置进样,并监测每个校准品检测值与理论值的偏倚,以明确在大样本量分析中的校准漂移情况。
校准确认是采用与检测临床标本相同的测量程序,分析在报告范围内已知待测物浓度的标本或商品化室间质量评价(external quality assessment,EQA)质控物以确认仪器或检测系统的校准,验证正在使用的校准曲线在检测患者标本时依然有效。建议在变更标准品批次后、确认不同分析批之间的校准有效性时,开展校准确认。校准确认品应与实际患者标本相同或具有相似的性质,并与患者标本进行相同的前处理。与患者标本基质不同的质控品和校准品不可作为校准确认品。
建议9 实验室应对每个分析批进行校准,并监测每个校准品浓度检测值与理论值的偏倚。
3. 室内质量控制
血清(浆)类固醇激素LC-MS/MS测量程序室内质控的难点是获取与患者标本基质相近且稳定性好的质控品。对于多组分分析的血清(浆)类固醇激素LC-MS/MS测量程序,应优先选择生产质控严格、稳定性明确,并同时包含多个待测组分的商品化质控品。使用经处理的血清(浆)、冻干或合成基质质控品的一个明显缺点是,因与患者标本基质不完全相同而产生不同的质谱响应。而未添加分析物的患者血清(浆)质控品可能在评估测量程序性能时比经过处理的质控品更可靠。如通过将类固醇纯溶液标准品添加入基质制备质控品,用于制备质控品的类固醇标准品批号及基质应有别于制备校准品的类固醇标准品及基质。另外,实验室可使用低、中、高浓度的单个或混合患者样本作为质控品。为了保证质控结果解读的一致性,质控样品应大批量制备,分装储存,并明确质控品的储存稳定性及与患者标本基质的一致性。
实验室应自行确定质控物靶值及最大允许不精密度( 表4 ),将质控物放置在每一分析批内和分析批间的不同位置检测,以监测测量程序的批内、批间漂移情况。可参考《临床检验定量测定室内质量控制 WS/T641-2018》建立测量程序的质控方案和失控规则(如1 3 s 、3 2 s 等),以及失控后处理措施,如分析批内质控不合格,应复测标本。
建议10 实验室应优先选择质量可靠、与患者标本基质一致的质控物,确定质控物靶值及最大允许不精密度,建立质控方案、失控规则和处理措施。
4. 分析批设置
血清(浆)类固醇激素LC-MS/MS测量一般分批进行,分析批的长度取决于系统校准稳定性和成本效益。一个典型的分析批应包含校准品、质控品、患者样本、空白样品、校准确认品(用于验证校准曲线的有效性,非必需)。实验室通过校准曲线、质控和校准确认监测每个分析批的有效性。当检测量大于2×96个时,建议每检测批次(96个/批次)都包含校准品、质控品和空白样本。实验室应确定并文件化血清(浆)类固醇激素LC-MS/MS测量程序的分析批长度 。
建议11 实验室应根据血清(浆)类固醇激素LC-MS/MS测量系统的稳定性和成本效益确定分析批的长度,并通过校准曲线、质控和校准确认监测每个分析批的有效性。
5. 能力验证/室间质量评价
由于血清(浆)类固醇激素LC-MS/MS检测程序标准化不足,基于分组数据进行测量结果一致性评估的EQA计划价值有限。正确度验证计划可同时监测测量程序的正确度和一致性,实验室应定期(1~2次/年)参加国家卫生健康委和/或省级临床检验中心正确度验证计划,如卫生健康委临床检验中心组织的类固醇激素正确度验证。正确度验证计划使用经最少程序处理的临床样本,通过参考方法对类固醇激素定值后,用于评估参评实验室LC-MS/MS测量程序的正确度和量值溯源性。对无正确度验证和室间质量评价计划的类固醇激素LC-MS/MS检测项目,实验室需定期(如2次/年)进行实验室间比对,并应优先选择通过ISO15189认可的实验室,以保证实验室间结果的一致性。
建议12 实验室应定期(1~2次/年)参加国家卫生健康委和/或省级临床检验中心组织的类固醇激素检测能力验证计划,无能力验证计划的项目需定期(2次/年)进行实验室间比对。
(五)数据收集及分析
实验室应建立患者样品、空白样品、校准品和质控品的数据处理、峰积分的标准操作程序,并在每一次临床检测中保持一致。数据处理软件应带有审核追踪功能可查询每个样品的数据处理方法。
1. 校准曲线接受原则
以校准品/内标物浓度比值为 X轴、分析物/内标物响应比值为 Y轴,构建校准曲线,将每个患者样品、质控品和空白样品的分析物/内标物响应比值代入校准曲线方程计算被测物浓度。分析患者标本时使用的校准曲线回归方法应与进行测量程序性能验证时使用的方法保持一致,大多数情况采用线性回归。如果校准曲线数据方差不同质(不同浓度点差异不同),推荐使用1/ x或1/ x 2权重回归分析以使低浓度校准点的偏倚在可接受范围。实验室应通过观察每个校准浓度点的相对偏差或总相对偏差选择合适的权重分析方法。
血清(浆)类固醇激素LC-MS/MS测量程序性能验证应明确校准曲线可接受标准:使用校准曲线计算出的校准品浓度与理论浓度之间偏倚可接受范围为85%~115%(LOQ浓度点:80%~120%)。确定校准曲线斜率和截距的可接受标准,计算相关系数、确定其接受范围(通常需>0.99),并应用于常规分析的评估。校准曲线的可接受标准应与测量程序性能(如准确度)匹配。
建议13 血清(浆)类固醇激素LC-MS/MS测量校准曲线计算的校准品浓度与理论浓度之间偏倚的可接受范围推荐设置为85%~115%(LOQ浓度点:80%~120%)。
2. 色谱峰积分
应在类固醇激素LC-MS/MS常规检测中通过优化积分参数完成色谱峰的自动积分,以尽量避免操作人员手动积分导致的不一致性。通常使用3倍LOQ浓度类固醇激素样品的色谱峰优化自动积分参数。对色谱峰进行平滑处理可提升积分准确性,仪器背景杂质信号过高或色谱峰采集数据点不足可导致色谱峰不够平滑。但色谱峰过度平滑会导致峰形变宽和丢失细节,如将肩峰平滑进待测物的色谱峰,将影响待测物定量结果准确性。对于采样率较慢的系统,可使用成组平滑方法减小背景杂质信号的影响。经验性色谱峰平滑参数应在所有样品分析中保持一致。
建议14 应尽量通过优化积分参数完成每个待测类固醇激素的色谱峰自动积分,避免手动积分,实际标本检测需统一峰积分、平滑参数。
3. 色谱峰核查
在类固醇激素LC-MS/MS测量程序性能验证时,应建立色谱峰保留时间、背景杂质信号强度、峰形和峰分辨率的核查规则。理想的色谱峰是对称的且基线分离完整。如果一个分析批内有样品色谱峰基线分离不完整、峰形变宽或裂分,排除管路连接不正确的原因,应考虑更换色谱柱。实验室必须核查色谱峰的保留时间以确保待测物分析峰的正确积分,并在标准操作流程中明确保留时间的最大允许漂移范围,分析批间的变化应不超过±2.5%。样品中分析物色谱峰的保留时间应与校准品的保留时间一致。实验室可采用人工核查色谱峰,也可通过在仪器控制软件中设置色谱峰核查参数自动完成。如果使用自动色谱峰核查,实验室需验证自动核查参数及流程的有效性,同时明确需人工介入核查的情况。
建议15 实验室应建立每个待测类固醇激素的色谱峰保留时间、背景杂质信号强度、峰形、峰分辨率的核查规则和允许范围。
4. 内标峰面积核查
通过计算每个类固醇激素LC-MS/MS检测样品内标峰面积与校准品平均峰面积的比值确定每个样品的内标峰面积回收率。内标回收率用于校正分析物提取回收率,每个样品内标峰面积不同是可接受的,但在性能验证时应建立样品之间内标峰面积变动的最大可接受范围。样品内标峰面积回收率出现明显降低提示前处理效率低或存在其他可导致离子抑制的干扰物或存在干扰内标定量离子对的杂质峰。对于内标峰面积比前后样品少2/3或50%的样品,应复检。明显升高的回收率提示内标峰包含干扰峰,也需复检。可通过内标峰面积随进样量变化作图,识别过低或过高的回收率。
建议16 实验室应日常监测每个待测类固醇激素的内标峰面积在标准品、质控物及标本间的波动,建立内标峰面积波动的最大可接受范围。
5. 定性离子对监测
类固醇激素LC-MS/MS常规检测中,一个离子对用于定量分析(定量离子对),另一个离子对用于定性分析(定性离子对)。定性离子对用于分析物定性,在识别样品干扰物中发挥重要作用。定量离子对峰面积与定性离子对峰面积的比值在不同样品间应保持一致,如果发生变化则提示存在干扰物质。如果无法检出定量或定性离子对则提示样品中不存在该分析物或存在干扰物,应进一步分析原因。应同时评估分析物和内标物的定量离子对/定性离子对比值。定性离子对应在整个测量区间有稳定的响应,避免使用脱水分子、脱乙酰基、脱甲基或加合物的子离子设置定性离子对。测量程序性能验证时应建立定量/定性离子对比值差异的可接受范围(如±30%),并在每一个样品检测中予以监测。
建议17 实验室应日常监测每个待测类固醇激素的定量/定性离子对峰面积比值在标准品、质控物及标本间的波动,并设置最大可接受范围。
三、血清(浆)类固醇激素LC-MS/MS检验后质量保证
1.数据存储
实验室应保存血清(浆)类固醇激素LC-MS/MS分析产生的完整原始数据和处理数据,包括测量程序使用的色谱和质谱参数设置、每个离子对的色谱和质谱数据等,必要时使用独立系统备份数据。
2.参考范围
由于抗原抗体非特异性反应及与LC-MS/MS测量结果的偏差,采用免疫法建立的类固醇激素参考范围一般不适用于LC-MS/MS测量程序,然而我国目前尚未建立公认统一的类固醇激素LC-MS/MS检测参考范围,实验室可参考CLSI EP28针对目标检测人群验证国外权威机构建立的参考范围 ,不同类固醇激素需按性别、年龄和/或月经周期分组,例如绝经前妇女的雌二醇、雌酮和雌三醇的浓度因月经周期或妊娠阶段的不同而有较大差异。
建议18 实验室可针对目标检测人群验证国外权威机构建立的类固醇激素LC-MS/MS参考范围,推荐建立中国人群的参考范围。
3.结果解读及报告
肾上腺皮质激素代谢终产物醛固酮和皮质醇浓度增高分别和醛固酮增多症和皮质醇增多症(库欣综合征)密切相关;17α-羟孕烯醇酮、17α-羟孕酮及其雄激素代谢产物(如脱氢表雄酮、雄烯二酮)水平的异常往往与女性PCOS、高雄激素血症及性发育异常等内分泌疾病相关;绝经后女性雌二醇检测是乳腺癌发病风险评估的关键;对女性和青春期前儿童体内睾酮的检测是鉴别儿童性早熟、女性高雄激素血症和PCOS的关键;对峰谷游离皮质醇的准确检测可有效辅助诊断库欣综合征;对17α-羟孕酮、雄烯二酮、孕烯醇酮、孕酮、17α-羟孕烯醇酮、11-脱氧皮质酮和18-羟皮质酮的准确检测是确定CAH亚型的重要依据。此外,血清(浆)类固醇激素检测结果的解读应基于目标患者或人群的基本信息,如性别、年龄、生理期、昼夜节律及立卧位等,对结果解读具有重要参考意义。因此,实验室应为类固醇激素质谱检测的目标人群建立个性化的结果解读规则。为了报告的准确性,类固醇激素结果的解读还应结合类固醇代谢通路和临床初步诊断。
建议19 实验室应结合患者临床信息、方法性能、临床预期用途、类固醇代谢通路解读和报告血清(浆)类固醇激素LC-MS/MS检测结果。
血清(浆)类固醇激素LC-MS/MS检测在精确评估类固醇激素水平、诊断类固醇激素失衡相关疾病(如CAH、肾上腺功能不全、高雄激素血症等)、监测治疗效果中发挥着越来越重要的作用。本共识对血清(浆)类固醇激素LC-MS/MS检测全流程进行了详细说明,包括标本采集、保存、运输及前处理的检验前过程,LC-MS/MS定量分析方法、分析性能指标、质量保证、数据收集及分析的检验中过程,以及数据存储、参考范围、结果解读及报告的检验后过程,并提出19项针对性建议供实验室参考。本共识旨在规范我国血清(浆)类固醇激素LC-MS/MS检测程序,提升其检测质量和结果一致性,推动其临床应用。
执笔人:李霖(四川省医学科学院 四川省人民医院临床医学检验中心),蒋黎(四川省医学科学院 四川省人民医院临床医学检验中心),郭玮(复旦大学附属中山医院检验科),邱玲(中国医学科学院 北京协和医院检验科)
专家组成员(以姓氏拼音排序):曹正(首都医科大学附属北京妇产医院检验科),戴锦娜(中国医科大学附属第一医院检验科),俸家富(绵阳市中心医院检验科),郭启雷(山东英盛生物技术有限公司),郭玮(复旦大学附属中山医院检验科),郭晓兰(川北医学院附属医院检验科),黄庆[陆军军医大学附属大坪医院(陆军特色医学中心)检验科],蒋黎(四川省医学科学院 四川省人民医院临床医学检验中心),蒋廷旺(常熟市第二人民医院转化医学科),柯江维(江西省儿童医院医学检验科),李霖(四川省医学科学院 四川省人民医院临床医学检验中心),李卿(上海市临床检验中心参考测量实验室),李水军(上海市徐汇区中心医院中心实验室),李艳妍(吉林大学第一医院检验科),廖璞(重庆市人民医院检验科),刘华芬(杭州凯莱谱精准医疗检测技术有限公司),刘靳波(西南医科大学附属医院医学检验科),卢丽萍(中国医科大学附属盛京医院检验科),闵迅(遵义医科大学附属医院医学检验科),倪君君(和合诊断集团研究院),聂滨(宜宾市第二人民医院检验科),潘柏申(复旦大学附属中山医院检验科),邱玲(中国医学科学院 北京协和医院检验科),王成彬(解放军总医院检验科),王书奎(南京医科大学附属南京医院医学检验科),夏勇(广州医科大学附属第三医院检验科),徐元宏(安徽医科大学第一附属医院检验科),张传宝(国家卫生健康委临床检验中心生化室),张华(贵州省人民医院检验科),赵蓓蓓(金域医学临床质谱检测中心)
本文引用来源:中国质谱学会临床质谱专家委员会. 血清(浆)类固醇激素液相色谱-串联质谱检测质量保证专家共识.















